
QUALIDADE DE ÓLEOS COMPOSTOS POR SOJA (Glycine max L.) E MAMÃO (Carica papaya L.) SUBMETIDOS À ESTOCAGEM ACELERADA EM ESTUFA
Capítulo de livro publicado no livro do “ÓLEOS VEGETAIS: PROPRIEDADES FÍSICO-QUÍMICAS, BIOATIVAS E ANTIOXIDANTES“. Para acessa-lo clique aqui.
Este capítulo de livro foi escrito por:
Carolina Médici Veronezi1; Neuza Jorge2*
1Pós-doutoranda do Depto de Engenharia e Tecnologia de Alimentos, Instituto de Biociências, Letras e Ciências Exatas, Universidade Estadual Paulista “Júlio de Mesquita Filho” – UNESP.
2Docente do Depto de Engenharia e Tecnologia de Alimentos, Instituto de Biociências, Letras e Ciências Exatas, Universidade Estadual Paulista “Júlio de Mesquita Filho” – UNESP; *E-mail: [email protected].
Resumo: Um grande volume de sementes de frutos, com elevado potencial nutricional, é gerado pela agroindústria, e que, na maioria das vezes, tem uso limitado somente para a indústria de rações animais ou são descartadas causando sérios danos ambientais. Assim, o trabalho teve como objetivo monitorar a estabilidade dos óleos de soja (S), mamão (Ma), SMa25 (75:25 p/p) e SMa50 (50:50 p/p) sob estocagem acelerada em estufa (60°C/12 dias). As propriedades físico-químicas dos óleos apresentaram diferença significativa, e o óleo de soja obteve maior degradação, representada pela quantidade de peróxidos (57,0 meq/kg) e, consequentemente, valor totox (120,5). Por outro lado, constatou-se que entre os óleos compostos, o SMa50 apresentou menor degradação, devido a maior adição de óleo de mamão. Em relação ao perfil de ácidos graxos, se sobressaiu o ácido oleico nos óleos, exceto no de soja que mostrou ser predominantemente composto por ácido linoleico. Ao final da estocagem em estufa houve aumento na quantidade de ácidos graxos saturados e/ou monoinsaturados e diminuição dos poli-insaturados. O isômero γ-tocoferol se destacou nos óleos de soja e nos compostos. Entre os óleos compostos, o SMa25 apresentou elevadas quantidades de tocoferóis totais, em decorrência da maior quantidade de óleo de soja. Após a estocagem, os tocoferóis totais diminuíram, exceto para o óleo de mamão. Dessa forma, as sementes de mamão apresentam grande potencial como matéria-prima para a extração de óleos, e constatou-se que com 50% de adição de óleo de mamão, maior foi a estabilidade do óleo de soja, quando estocado a 60°C/12 dias em estufa.
Palavras-chave: estabilidade oxidativa; óleos especiais; propriedades físico-químicas; sementes
INTRODUÇÃO
Na alimentação humana, os óleos vegetais contribuem com 30-40% do total de energia consumida, além de apresentarem funções metabólicas, como o envolvimento na formação de hormônios esteroides; nas reações enzimáticas e transmissão de impulsos nervosos; no fornecimento de ácidos graxos essenciais, carotenoides e esteróis; transporte de vitaminas lipossolúveis (A, D, E, K). Uma vez que nenhum óleo refinado tem uma composição ideal de ácidos graxos e visto que os processos de hidrogenação, interesterificação e diminuição de ácido graxo α-linolênico apresentam alguns inconvenientes, surgiram os óleos compostos (O’BRIEN, 2008).
O óleo de soja, dentre muitas aplicações, é utilizado no preparo de assados, margarinas, maioneses e, preferencialmente, como base para frituras (SAVVA; KAFATOS, 2015). É composto por cerca de 85% de ácidos graxos insaturados, tocoferóis e fitosteróis, como β-sitosterol (52%), campesterol (25%) e estigmasterol (23%) (GHAZANI; MARANGONI, 2015). Em comparação a outros óleos vegetais, o de soja apresenta algumas vantagens como a capacidade de ser parcialmente hidrogenado; facilidade de remoção de fosfatos, restos de metais e sabões que permanecem após a extração; e presença de antioxidante natural. Por outro lado, é um óleo com baixa estabilidade oxidativa, devido à elevada presença de ácidos linoleico e α-linolênico (GANESAN; SUKALINGAM; XU, 2017).
O mamão ou papaia é amplamente utilizado em dietas alimentares, por ter sabor doce, consistência suave, cor atrativa e elevado valor nutritivo, sendo excelente fonte de cálcio, magnésio, fósforo, ferro, vitamina C e carotenoides, como licopeno, β-criptoxantina e β-caroteno (SILVA JUNIOR et al., 2018). Também possui substâncias, como o isotiocianato de benzila, com ação antihelmíntica e antifúngica, além de compostos quimioprotetores, que podem agir como inibidores no desenvolvimento de câncer de pâncreas e pulmão (LEE; LEE; SU, 2011). Embora a população consuma apenas o fruto, as várias partes do mamoeiro, como as folhas, o látex, as flores, a casca e as sementes são usadas para fins medicinais, devido à presença de compostos bioativos (KRISHNA; PARIDHAVI; PATEL, 2008).
As sementes do mamão podem ser utilizadas como produtos alimentícios ou matéria-prima para a extração de óleos, pois são ricas em lipídios (25-30%), proteínas (25-28%), fibras (28-30%) e são fontes de magnésio, cálcio e ferro. Possuem também glucosinolatos e alcaloides com propriedades quimiopreventivas, antibacterianas e anticancerígenas (KUMAR; SREEJA DEVI, 2017). O óleo de sementes de mamão é rico em ácidos graxos monoinsaturados (70-79%), embora tenha quantidades significativas de ácidos palmítico (14-17%) e esteárico (3-5%). Também possuem substâncias benéficas ao organismo humano, como os fitosteróis (6,8 mg/kg), se destacando β-sitosterol, campesterol e estigmasterol; os carotenoides β-criptoxantina (4,29 mg/kg) e β-caroteno (2,76 mg/kg); os compostos fenólicos totais (156-528 mg EAG/g), e apresentam elevado valor comercial (MALACRIDA; KIMURA; JORGE, 2011).
Com intuito de explorar e utilizar os recursos naturais presentes em nosso país, em especial as sementes de frutos geradas pela agroindústria, que geralmente são descartadas causando sérios danos ambientais e/ou utilizadas como ração animal, o objetivo deste trabalho foi monitorar a estabilidade dos óleos de soja, mamão e os compostos formulados em diferentes proporções sob estocagem acelerada em estufa (60°C/12 dias).
MATERIAL E MÉTODOS
Material
Foram utilizadas sementes de mamão (Carica papaya L.), variedade Formosa (cultivar Mamão-formosa), cedidas por uma empresa localizada em Jundiaí-SP. Após o recebimento, as sementes foram lavadas com água destilada para a retirada dos restos de polpa visivelmente presentes. Na sequência, foram secas em estufa com circulação de ar forçado (modelo MA 035, Marconi) a 40 ± 0,5°C/48 h e armazenadas ao abrigo de luz em recipientes de vidro vedados com tampas de rosca para a extração dos óleos.
Os óleos das sementes foram extraídos pelo método de Soxhlet utilizando éter de petróleo como solvente. Após a extração, a miscela foi filtrada para retirada de interferentes provenientes das sementes. Também foi utilizado o óleo de soja sem adição de antioxidantes sintéticos adquirido no mercado de São José do Rio Preto-SP. A seguir, foram formulados os óleos compostos, conforme mostra a Tabela 1.

Estocagem acelerada em estufa
Cinquenta gramas de cada óleo foram colocados em recipientes de vidro âmbar, com relação superfície/volume de 0,4/cm e submetidos à estocagem acelerada em estufa a 60 ± 5°C/12 dias. Após a estocagem, as amostras foram retiradas da estufa e acondicionadas à temperatura de -18°C para as análises posteriores.
Métodos
Para as determinações de ácidos dienoicos conjugados, índices de peróxidos, ρ-anisidina foram utilizados os métodos da AOCS (2009). O valor total de oxidação (Totox) foi calculado pela relação existente entre o valor do índice de peróxidos (IP) e ρ-anisidina (IρA), por meio da equação: Totox = 2 (IP) + (IρA), conforme Shahidi (2005). Os índices de refração, iodo e estabilidade oxidativa foram determinados também pelos métodos oficiais da AOCS (2009). A estabilidade oxidativa foi realizada em Rancimat (modelo 743, Metrohm Ltda., Herisau, Switzerland) a 110°C e fluxo de ar de 20 L/h.
O perfil de ácidos foi realizado por cromatografia em fase gasosa dos ésteres metílicos, conforme o método da AOCS (2009). Foi utilizado um cromatógrafo a gás (modelo CG 3900, Varian, Walnut Creek, Estados Unidos) com coluna capilar de sílica fundida (CP-Sil 88 de 60 m de comprimento, com diâmetro interno de 0,25 mm e espessura do filme de 0,20 µm), detector de ionização de chama, injetor split e amostrador automático. O gás de arraste foi o hidrogênio com velocidade linear de 30 mL/min, a temperatura da coluna iniciada em 90°C/4 min., com aumento de 10ºC/min. até 195°C e mantida em isoterma por 16 min. As temperaturas utilizadas no injetor e detector foram 230 e 250ºC, respectivamente e razão de divisão de 1:30. A identificação dos ácidos graxos foi realizada por comparação dos tempos de retenção das amostras teste com o tempo de retenção de padrões cromatográficos de ésteres metílicos. Utilizou-se como padrão uma mistura composta de 37 ésteres metílicos de ácidos graxos (Supelco, Bellefonte, Estados Unidos), de C4:0 a C24:1, com pureza entre 99,1 e 99,9%. Por meio de uma distribuição randômica, que leva em consideração o perfil de ácidos graxos, foi determinada a composição provável de triacilgliceróis utilizando o programa computacional desenvolvido por Antoniosi Filho, Mendes e Lanças (1995). Grupos com concentração total de triacilgliceróis menor que 0,5% não foram considerados.
Carotenoides totais foram determinados por espectrofotometria de varredura segundo metodologia descrita por Rodriguez-Amaya (2004). A quantificação foi calculada por meio da absorção no comprimento de onda de absorção máxima e valor de absortividade de 2592 em éter de petróleo, utilizando a equação: μg/g de óleo = [(Abs x 25 x 1000)/2592 x P], onde Abs representa a absorvância da amostra em λ = 450-477 nm, e P é o peso da amostra de óleo.
Os compostos fenólicos totais foram extraídos de acordo com o método proposto por Parry et al. (2005) e analisados conforme metodologia descrita por Singleton e Rossi (1965), utilizando reagente de Folin-Ciocalteu e curva padrão de ácido gálico (R2 = 0,9998), sendo detectados a λ = 765 nm em espectrofotômetro (modelo UV-VIS mini 1240, Shimadzu, Chiyoda-ku, Tóquio, Japão) e os resultados expressos em mg EAG/g.
A composição de tocoferóis, utilizando o método da AOCS (2009) foi realizada em cromatógrafo líquido de alta eficiência (modelo 210-263, Varian, Walnut Creek, Estados Unidos), com detector de fluorescência, coluna de aço inox empacotada com sílica (100 Si, Microsorb, Varian, Walnut Creek, Estados Unidos) e comprimentos de ondas de excitação e emissão de 290 e 330 nm, respectivamente. Os valores das concentrações foram calculados em base da área dos picos de excitação da leitura e expressos em valores de cada isômero separadamente. Uma curva padrão de α-, β-, γ- e δ-tocoferol (Supelco, Bellefonte, Estados Unidos) com elevado grau de pureza foi elaborada para expressar o teor de tocoferóis em mg/kg.
Análise estatística
Foi utilizado o delineamento inteiramente casualizado em esquema fatorial. Os resultados obtidos das determinações analíticas foram submetidos à análise de variância e as diferenças entre as médias foram testadas a 5% de probabilidade pelo teste de Tukey, por meio do programa ESTAT, versão 2.0 (BANZATTO; KRONKA, 2006).
RESULTADOS E DISCUSSÃO
Os testes acelerados baseiam-se na elevação da temperatura para aumentar a velocidade de reação de oxidação. Esse teste possibilita conhecer a vida útil dos óleos, visto que os resultados fornecidos apresentam boa correlação com a avaliação efetuada em condições de estocagem à temperatura ambiente (GÓMEZ-ALONSO et al., 2007). Foi constatado menor percentual de ácidos dienóicos conjugados no óleo de mamão (0,3%), contribuindo para a redução de 17% de ácidos dienóicos nos óleos compostos em ambas proporções, quando comparado com o óleo de soja (Tabela 2). Após a estocagem, com exceção do óleo de mamão, os ácidos dienoicos aumentaram, sobretudo nos óleos de soja e SMa25, com 0,8%. Verificou-se que no óleo de mamão não foram detectados peróxidos, e que o óleo composto SMa50 apresentou menor quantidade de peróxidos do início ao final do processo e foi o único que, após a estocagem, não ultrapassou os valores máximos de peróxidos estabelecido pelo Codex Alimentarius Commission (2009), 10 e 15 meq/kg para óleos refinados e brutos, respectivamente.
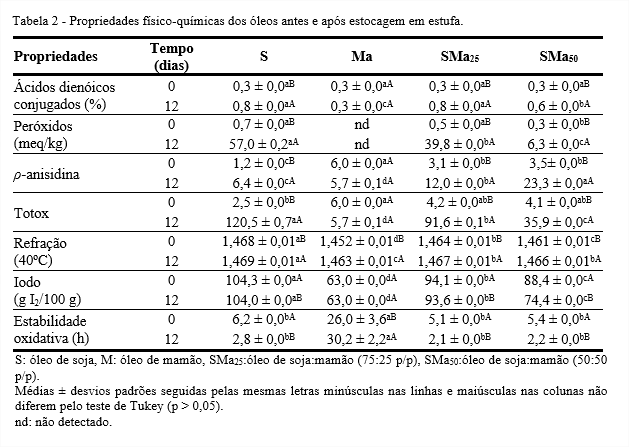
Os compostos primários, com o decorrer do tempo se transformam em outras substâncias, como aldeídos. Os óleos podem ser qualificados pelos valores dos índices de ρ-anisidina e totox, sendo considerados de boa qualidade aqueles que se encontram com valores inferiores a 10 (BERSET; CUVELIER, 1996; GUILLÉN; CABO, 2002). Pode-se inferir que, antes da estocagem, os óleos apresentaram boa qualidade, visto que a maior quantidade encontrada, em ambas as análises, foi no óleo de mamão (6,0). Porém, após a estocagem, houve aumento nos valores de ρ-anisidina e totox, exceto para o óleo de mamão, que se manteve constante. Os óleos compostos e o de soja ultrapassaram o valor considerado adequado para a análise de ρ-anisidina e totox, respectivamente.
Pelo índice de refração, observou-se que o óleo de soja é o mais insaturado, com 1,468-1,469, influenciando na composição dos óleos compostos. O mesmo comportamento foi observado em relação ao índice de iodo, visto que ambas as análises estão relacionadas com o grau de insaturação dos ácidos graxos. Antes da estocagem, o óleo de mamão mostrou maior estabilidade oxidativa (26 h), no entanto, não influenciou na formulação dos óleos compostos, visto que os mesmos não apresentaram diferença significativa em relação ao óleo de soja. Aos 12 dias de estocagem, houve redução da estabilidade, exceto para o óleo de mamão, que se mostrou mais estável (30,2 h).
Em relação ao perfil de ácidos graxos, entre os saturados, o ácido palmítico se destacou nos óleos, com médias de 21,67 a 24,13%, ao se comparar com a quantia de esteárico. Contudo, maior valor foi encontrado no óleo de mamão (Tabela 3).
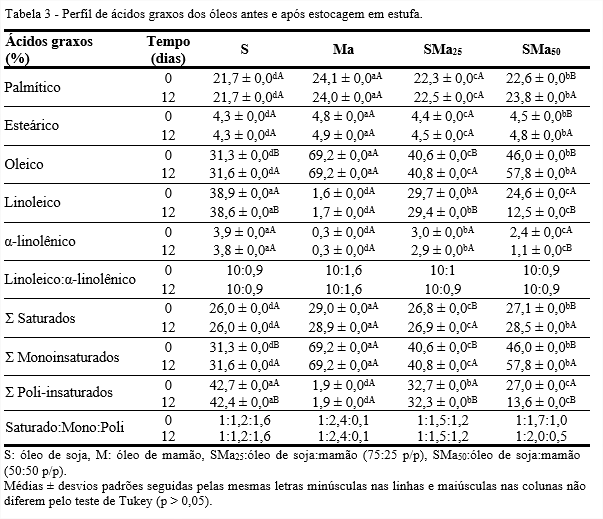
- SMa50 que apresentou aumento de 5,4%. O óleo de mamão também apresentou maior quantidade de ácido esteárico durante a estocagem e o composto SMa50 teve aumento de 6% em 12 dias.
O ácido oleico foi encontrado em maior quantidade no óleo de mamão, aproximadamente 69%. Devido a isso, os óleos SMa25 eSMa50 mostraram aumento de 30 e 47% de ácido oleico, respectivamente, em relação ao óleo de soja. Com exceção do óleo de mamão, que permaneceu constante, as quantidades de ácido oleico nos óleos aumentaram com o tempo de estocagem, por causa da quebra de ligações duplas de outros ácidos graxos. O óleo de soja se destacou com maiores quantidades de ácidos linoleico (38,9-38,6%) e α-linolênico (3,9-3,8%). Porém, com a adição do óleo de mamão, foi possível verificar reduções de 37 e 24% de ácido linoleico nos óleos SMa50 e SMa25, respectivamente, antes da estocagem.
Como os ácidos graxos linoleico e α-linolênico competem pelas enzimas envolvidas nas reações de dessaturação e alongamento de cadeia é importante conhecer a proporção que se encontram nos alimentos (ENSER et al., 2001; SIMOPOULOS, 2008). A relação ideal de ácidos ω6:ω3 para que o óleo seja considerado adequado para consumo varia entre cada país, como por exemplo, para Canadá é de 4:1 a 10:1; EUA de 2:1 a 3:1 e Japão é 2:1 a 4:1. Por outro lado, a Organização Mundial de Saúde considera a razão ideal de 5:1 a 10:1 (MARTIN et al., 2006; WHO, 2008). Com exceção do óleo de mamão, os demais óleos apresentaram proporção aproximadamente de 10:1, independente do tempo de estocagem.
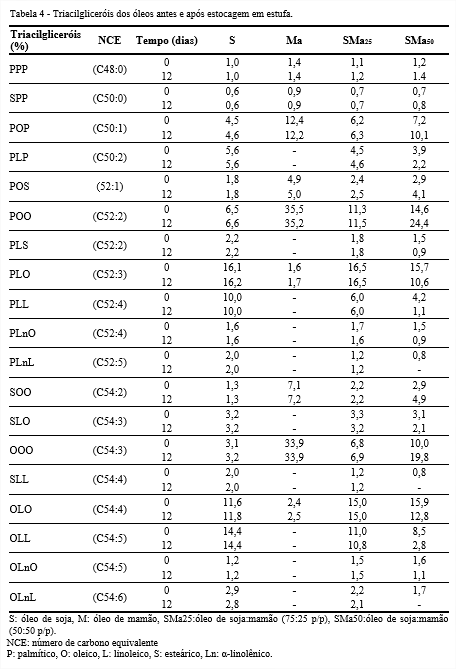
O óleo de mamão mostrou ser predominantemente monoinsaturado, enquanto o de soja apresentou maior quantidade de ácidos poli-insaturados. Aos 12 dias, a quantidade de ácidos monoinsaturados aumentou, enquanto a de poli-insaturados diminuiu nos óleos, exceto no de mamão que se mostrou estável. Quanto à relação entre os ácidos graxos saturados, mono e poli-insaturados, os óleos compostos, inicialmente, mostraram valores aproximados aos considerados ideais pela Organização Mundial da Saúde (1:1,5:1) (WHO, 2008). Porém, com 12 dias de estocagem, somente o SMa25 manteve-se dentro dessas quantidades preconizadas. Com base nos ácidos graxos, foi obtido o perfil de triacilgliceróis, como mostra a Tabela 4. Nota-se que os óleos apresentaram 19 tipos de triacilgliceróis, exceto o de mamão que mostrou apenas 9 tipos, com destaque para o POO, devido elevada porcentagem de ácido oleico e baixas quantidades de ácidos linoleico e α-linolênico em
relação ao de soja. Os óleos SMa50 e SMa25 mostraram quantidades semelhantes de PLO e OLO, inicialmente, evidenciando a influência do óleo de soja sobre o do mamão.
No óleo de soja não foram detectados carotenoides totais, por se tratar de um óleo refinado (Tabela 5). Por outro lado, incialmente, o óleo de mamão mostrou elevada quantidade de carotenoides totais (38,1 μg/g), influenciando os óleos SMa50 e SMa25 que apresentaram 8,4 e 22,8 μg/g, respectivamente. Porém, após a estocagem, a quantidade de carotenoides do óleo de mamão reduziu 79%, influenciando os óleos compostos.
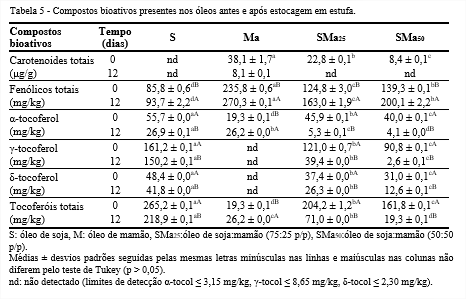
Antes da estocagem, o óleo de mamão mostrou elevada quantidade de compostos fenólicos totais (235,8 mg/kg) em comparação aos demais, por ser um óleo bruto, contribuindo por elevar em 62% a quantidade desses compostos no óleo de soja, uma vez que o SMa50 apresentou 139,3 mg/kg. Com a estocagem, aos 12 dias, houve aumento de compostos fenólicos nos óleos, posssivelmente devido à reação do reagente de Folin-Ciocalteu com outros grupos fenóis (PRIOR; WU; SCHAICH, 2005).
Os isômeros α-, γ- e δ-tocoferóis foram detectados nos óleos, exceto no de mamão. A quantidade de α-tocoferol foi maior no óleo de soja (55,7 mg/kg) e, consequentemente, no SMa25 (45,9 mg/kg) devido ser constituído por 75% de óleo de soja. Entre os isômeros, destacou-se o γ-tocoferol, que é muito importante, pois tem propriedades anti-inflamatórias, anticancerígenas, alivia colite moderada, além disso, em combinação com a cessação do tabagismo melhora a função endotelial vascular, dentre outras propriedades (JIANG et al., 2013). Com 12 dias de estocagem, verificou-se redução na quantidade de tocoferóis totais, exceto no óleo de mamão.
CONCLUSÕES
Os óleos submetidos à estocagem acelerada em estufa apresentaram modificações nas propriedades físico-químicas com o tempo, porém o óleo de mamão foi o que obteve menor degradação, visto que se manteve com valores de ρ-anisidina e totox constantes.
O ácido oleico se sobressaiu nos óleos, exceto no de soja que mostrou ser, predominantemente, composto por ácido linoleico. Ao final da estocagem em estufa houve aumento na quantidade de ácidos graxos saturados e/ou monoinsaturados e diminuição dos poli-insaturados.
Houve uma elevada redução nos teores de carotenoides dos óleos, exceto no óleo de mamão, que apresentou retenção de 21%. O isômero γ-tocoferol se sobressaiu nos óleos de soja e nos compostos. Entre os óleos compostos, o SMa25 apresentou elevadas quantidades de tocoferóis totais, devido a maior quantidade de óleo de soja. Ao final do processo, os tocoferóis totais diminuíram, exceto para o óleo de mamão, por ser um óleo bruto.
Assim, as sementes de mamão apresentam potencial como matéria-prima para a extração de óleos. Constatou-se que a estabilidade do óleo de soja foi aumentada com a adição de 50% de óleo de mamão, quando submetido a estocagem em estufa.
AGRADECIMENTOS
Os autores agradecem ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), pela bolsa de produtividade.
REFERÊNCIAS
AMERICAN OIL CHEMITS SOCIETY (AOCS). Official and tentative methods of the American Oil Chemists’ Society: including additions and revisions. 6. ed. Champaign, 2009.
ANTONIOSI FILHO, N. R.; MENDES, O. L.; LANÇAS, F. M. Computer prediction of triacylglycerol composition of vegetable oils by HRGC. Chromatographia, New York, v. 40, p. 557-562, 1995.
BANZATTO, D. A.; KRONKA, S. N. Experimentação agrícola. 4. ed. Jaboticabal: Funep, 2006. 237 p.
BERSET, C.; CUVELIER, M. E. Methods of estimating the degree of lipid oxidation and of measuring antioxidizing power. Sciences des Aliments, Dijon, v. 16, n. 3, p. 219-245, 1996.
CODEX ALIMENTARIUM COMMISSION. Codex Stan 210-1999: codex standard for named vegetable oils. Rome, 2009.
ENSER, M.; SCOLLAN, N.; GULATI, S.; RICHARDSON, I.; NUTE, G.; WOOD, J. The effects of ruminally-protected dietary lipid on the lipid composition and quality of beef muscle. In: INTERNATIONAL CONGRESS OF MEAT SCIENCE AND TECHNOLOGY, 47th, Poland. Anais…Poland: Meat and Fat Research Institute, 2001. v. 1, p. 12-13.
GANESAN, K.; SUKALINGAM, K.; XU, B. Impact of consumption and cooking manners of vegetable oils on cardiovascular diseases- a critical review. Trends in Food Science and Technology, v. 71, n. 1, p. 132-154, 2017.
GHAZANI, S. M.; MARANGONI, A. G. Healthy Fats and Oils. 2. ed. Elsevier Ltd., 2015.
GÓMEZ-ALONSO, S.; MANCEBO-CAMPOS, V.; SALVADOR, M. D.; FREGAPANE, G. Evolution of major and minor components and oxidation indices of virgen olive oil during 21 months storage at room temperature. Food Chemistry, London, v. 100, n. 1, p. 36-42, 2007.
GUILLÉN, M. D.; CABO, N. Fourier transform infrared spectra data versus peroxide and anisidine values to determine oxidative stability of edible oils. Food Chemistry, London, v. 77, n. 4, p. 503-510, 2002.
JIANG, Q.; JIANG, Z.; HALL, Y. J.; JANG, Y.; SNYDER, P. W.; BAIN, C.; HUANG, J.; JANNASCH, A.; COOPER, B.; WANG, Y.; MORELAND, M. Gamma-tocopherol attenuates moderate but not severe colitis and suppresses moderate colitis-promoted colon tumorigenesis in mice. Free Radical Biology and Medicine, Los Angeles, v. 65, n. 1, p. 1069-1077, 2013.
KRISHNA, K.; PARIDHAVI, M.; PATEL, J. A. Review on nutritional, medicinal and pharmacological properties of papaya (Carica papaya Linn.). Natural Product Radiance, v. 7, n. 4, p. 364-373, 2008.
KUMAR, N. S.; SREEJA DEVI, P. S. The surprising health benefits of papaya seeds: a review. Journal of Pharmacognosy and Phytochemistry. v. 6, n. 1, p. 424-429, 2017.
LEE, W. J.; LEE, M. H.; SU, N. W. Characteristics of papaya seed oils obtained by extrusion-expelling processes. Journal of the Science of Food and Agriculture, London, v. 91, n. 1, p. 2348-2354, 2011.
MALACRIDA, C.R.; KIMURA, M.; JORGE, N. Characterization of a high oleic oil extracted from papaya (Carica papaya L.) seeds. Ciência e Tecnologia de Alimentos, Campinas, v. 31, n. 4, p. 929-934, 2011.
MARTIN, C. A.; ALMEIDA, V. V.; RUIZ, M. R.; VISENTAINER, J. E. L.; MATSHUSHITA, M.; SOUZA, N. E.; VISENTAINER, J. V. Omega-3 and omega-6 polyunsaturated fatty acids: importance and occurrence in foods. Revista de Nutrição, Campinas, v. 19, n. 6, p. 761-770, 2006.
O’BRIEN, R. D. Fats and oils: formulating and processing for applications. 3 ed. Boca Raton: CRC Press, 2008. 680 p.
PARRY, J.; LUTHER, M.; ZHOU, K.; YURAWECZ, M. P.; WHITTAKER, P.; YU, L. Fatty acid composition and antioxidant properties of cold-pressed marionberry, boysenberry, red raspberry, and blueberry seed oils. Journal of Agricultural and Food Chemistry, Easton, v. 53, n. 6, p. 566-573, 2005.
PRIOR, R. L.; WU, X.; SCHAICH, K. Standardized methods for de determination of antioxidant capacity and phenolics in foods and dietary supplements. Journal of Agricultural and Food Chemistry, Easton, v. 53, n. 10, p. 4290-4302, 2005.
RODRIGUEZ-AMAYA, D. B. A guide to carotenoids analysis in food. Washington: ILSI Press, 2004. 71 p.
SAVVA, S. C.; KAFATOS, A. Vegetable oils: dietary importance. 1. ed. Elsevier Ltd., 2015.
SHAHIDI, F. Bailey’s industrial oil & fats products. 6 ed. New York: John Wiley & Son 2005. 3616 p.
SILVA JUNIOR, E. V.; MELO, L. L.; MEDEIROS, R. A. B.; BARROS, Z. M. P.; AZOUBEL, P. M. Influence of ultrasound nd vacuum assisted drying on papaya quality parameters. Food Science and Technology, London, v. 97, p. 317-322, 2018.
SIMOPOULOS, A. P. The importance of the omega-6/omega-3 fatty a ratio in cardiovascular disease and other chronic diseases. Experimental Biology and Medicine, New York, v. 233, n. 1, p.674-688, 2008.
SINGLETON, V. L.; ROSSI, J. A. Colorimetry of total phenolics with phosphomolybdic-phosphotungstic acid reagents. American Journal of Enology and Viticulture, Davis, v. 16, p. 144-158, 1965.
WHO. World Health Organization. Interim summary of conclusions & dietary recommendations on total fat & fatty acids. Geneva, Switzerland, 2008. (The joint FAO/WHO expert consultation on fats & fatty acids in human nutrition).
