CARATERIZAÇÃO FÍSICO-QUÍMICA DE ÓLEOS BRUTOS DE SOJA, CANOLA, MILHO E GIRASSOL
Capítulo de livro publicado no livro do “ÓLEOS VEGETAIS: PROPRIEDADES FÍSICO-QUÍMICAS, BIOATIVAS E ANTIOXIDANTES“. Para acessa-lo clique aqui.
Este capítulo de livro foi escrito por:
Irene Rodrigues Freitas1; Neuza Jorge2*
1Doutora em Engenharia e Ciência de Alimentos, Instituto de Biociências, Letras e Ciências Exatas, Universidade Estadual Paulista “Júlio de Mesquita Filho” – UNESP.
2Docente do Depto de Engenharia e Tecnologia de Alimentos, Instituto de Biociências, Letras e Ciências Exatas, Universidade Estadual Paulista “Júlio de Mesquita Filho” – UNESP; *E-mail: [email protected]
Resumo: Os óleos vegetais são derivados preponderantemente de algumas sementes, nozes, grãos de cereais e frutos e são usados com frequência na alimentação humana. Quimicamente, consistem em moléculas de triacilgliceróis, as quais são constituídas de três moléculas de ácidos graxos de cadeia longa ligados na forma de ésteres e uma molécula de glicerol. O objetivo deste estudo foi caracterizar os óleos brutos de soja, canola, milho e girassol de diferentes marcas do mercado brasileiro. Foi feita a caracterização físico-química por meio das análises de ácidos graxos livres, índice de peróxidos, índice de p-anisidina, valor totox, extinção específica, matéria insaponificável e índice de estabilidade oxidativa. Pelos resultados das análises físico-químicas, independentemente das marcas estudadas, considerando as médias gerais para os diferentes óleos brutos, pode-se apontar que o óleo de soja apresentou melhor qualidade do ponto de vista dos ácidos graxos livres (0,9%), índice de p-anisidina (1,3) e K270 nm (0,3); enquanto o de canola teve 7,0 de totox e 2,0 de K233 nm e, por último, o de milho com índice de peróxidos de 2,2 meq/kg. Os óleos de soja e milho exibiram maiores índices de estabilidade oxidativa (14 h), enquanto o óleo de milho obteve maior quantidade de matéria insaponificável (2,4%) que os demais, ambos os parâmetros são desejáveis, uma vez que a qualidade de um óleo vegetal depende muito da qualidade da matéria-prima.
Palavras-chave: análises físico-química; matéria-prima; óleos vegetais; qualidade
INTRODUÇÃO
A produção mundial de óleos vegetais segundo o USDA – United States Department of Agriculture, safra 2021/jan2022 foi estimada em 213,91 milhões de toneladas (USDA, 2021).
A qualidade de um óleo vegetal depende muito da qualidade da matéria-prima e de todas as etapas envolvidas na sua obtenção. Assim sendo, o controle de qualidade deve iniciar-se na semente oleaginosa ou fruto e estender-se nos processos de extração, refinação, transporte, distribuição e comercialização dos óleos.
Os óleos vegetais brutos são constituídos principalmente por triacilgliceróis (95-98%) e mistura complexa de outros componentes (2-5%). Estes constituintes minoritários são os ácidos graxos livres, monoacilgliceróis, diacilgliceróis, fosfolipídios, fitosteróis livres e esterificados, triterpenos, álcoois, tocoferóis, carotenoides, clorofila, hidrocarbonos, traços de íons metálicos (ferro, enxofre, cobre), produtos da oxidação, gomas, ceras, resíduos de pesticidas e compostos aromáticos, substâncias capazes de alterar cor, sabor e aroma (PRZYBYLSKI et al., 2005).
A qualidade de um alimento é o somatório de várias características, dentre elas, as propriedades físico-químicas, nutricionais e sensoriais. A segurança e autenticidade devem igualmente ser inseridas no leque de características de qualidade.
Não é comum o uso de óleos brutos pelos consumidores devido a sua cor e odor, características próprias destes óleos, geralmente indesejáveis, além de impurezas como ácidos graxos livres, hidrocarbonetos, glicolipídios, fragmentos de proteínas, resinas, gomas, mucilagens das sementes oleaginosas e materiais oxidados. Isto faz com que o processamento industrial seja necessário, além de eficiente, levando à remoção destes compostos desagradáveis primando pelo mínimo possível de efeito nos componentes desejados (tocoferóis, esteróis, fenóis) e pelo mínimo de perdas de óleo (CHEW; ALI, 2021).
Para avaliar a qualidade de um óleo vegetal devem ser consideradas várias características que podem ser determinadas por diferentes técnicas. No que se refere aos óleos vegetais, parâmetros físicos e químicos são analisados e utilizados para garantir a qualidade dos mesmos. Dentre os parâmetros mais comumente analisados, encontram-se os ácidos graxos livres, índices de peróxidos, ρ-anisidina, dienos conjugados, matéria insaponificável, estabilidade oxidativa, dentre outros. Tais parâmetros dependem da matéria-prima de origem, das condições climáticas e de cultivo, do processamento e da composição química dos triacilgliceróis os óleos brutos de soja, canola, milho e girassol por meio das características físico-quimicas.
MATERIAL E MÉTODOS
Material
Para esta pesquisa foram utilizados quatro óleos vegetais brutos, nomeadamente soja, canola, milho e girassol de cinco marcas comerciais (M1, M2, M3, M4 e M5). As amostras foram fornecidas pelas diferentes indústrias processadoras brasileiras de óleos vegetais. No Laboratório de Óleos e Gorduras, as amostras foram armazenadas em recipientes de vidro âmbar e inertizadas com gás nitrogênio e posteriormente armazenados em câmara de congelamento (-18ºC) e ao abrigo de luz até ao momento das análises.
Métodos
Determinações físico-químicas
Para determinar o teor de ácidos graxos livres, índice de peróxidos, índice de anisidina, extinção específica (K233nm e K270nm) e materia insaponificável, foram usados os métodos analíticos Ca 5a-40, Cd 8b-90, Cd 18-90, Ch 5-91 e Ca 6b-53, respectivamente, como descrito pela American Oil Chemists’ Society (AOCS, 2009). O valor total da oxidação (totox) foi calculado de acordo com Wanasundara e Shahidi (1994). A estabilidade oxidativa foi determinada de acordo com o método Cd 12b-92 da AOCS (2009), utilizando o equipamento Rancimat (modelo 743, Metrohm Ltda., Herisau, Switzerland) e as seguintes condições: 3 g de amostra; fluxo de ar de 20 L/h, temperatura de 110ºC e 60 mL de água destilada nos frascos contendo os eletrodos, cuja medida se baseia na condutividade elétrica dos produtos voláteis de degradação.
Análise estatística
O delineamento experimental utilizado foi inteiramente casualizado em esquema fatorial 5 x 4, com cinco marcas e quatro tipos de óleos. Foi realizado delineamento inteiramente casualizado quando havia dados não detectados. Os resultados foram expressos como valores de médias ± desvios padrões e foram avaliados empregando-se análise de variância (ANOVA) e teste de Tukey para verificar a diferença entre as marcas e óleos. Foi utilizado o software Assistat 7.7 beta. As diferenças foram consideradas significativas quando p ≤ 0,05.
RESULTADOS E DISCUSSÃO
A presença de ácidos graxos livres indica a qualidade da matéria-prima antes e durante o seu processamento para obtenção dos diferentes tipos de óleo. A porcentagem de ácidos graxos livres expressa em ácido oleico está apresentada na Tabela 1.
Dentre as marcas analisadas, para um mesmo tipo de óleo, verifica-se que para o óleo de soja bruto não houve variação significativa entre as marcas M2 e M4, e as porcentagens variaram entre 0,4% (M1) a 1,3% (M2).
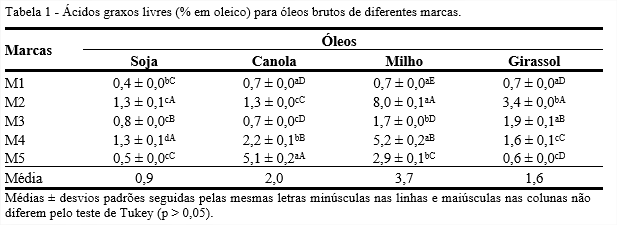
Para o óleo de canola bruto não houve diferença significativa (p > 0,05) entre as marcas M1 e M3. Observando o óleo de milho bruto, houve variações significativas entre todas as marcas. No óleo de girassol bruto destacou-se em porcentagem de ácidos graxos livres a marca M2, cujo valor máximo que alcançou 3,4%.
Pode-se observar que, entre os tipos de óleos da mesma marca, a marca M2 apresentou o maior teor de ácidos graxos livres para o óleo de milho (8,0%) e a marca M5 para o óleo de canola (5,1%). Ghazani, García-Lattas e Marangoni (2013) e Suliman, Jiang e Liu (2013) em seus estudos encontraram para os óleos brutos de canola e girassol teores superiores a 0,5%.
Altos valores de ácidos graxos livres obtidos nos óleos brutos podem estar associados à qualidade dos grãos e sementes utilizadas para a extração do óleo, ao teor de umidade retida nesses óleos brutos e ao tempo de armazenamento antes de serem submetidos à refinação. Esses fatores podem contribuir para as alterações químicas e, consequentemente, aumentar o teor de ácidos graxos livres, pois, a hidrólise de ligações ésteres, resulta na liberação de ácidos graxos livres. A hidrólise pode ser causada pela ação das lipases presentes nas sementes oleaginosas ou por lipases de origem microbiana, devido a elevadas temperaturas e umidade. Este constitui-se um dos problemas técnicos mais importantes na indústria de óleos (HUI, 1996; OSAWA; GONÇALVES; RAGAZZI, 2006).
Os menores percentuais de ácidos graxos livres foram encontrados nos óleos de soja para as marcas M1 e M5; canola para as marcas M1 e M3; milho para a marca M1 e girassol para as marcas M1 e M5. Dentre todas as marcas e todos os óleos analisados, o óleo de soja destacou-se por apresentar o menor teor de ácidos graxos livres na marca M1 com 0,4%, não diferindo da marca M5 com 0,5%.
De maneira geral, os baixos percentuais de ácidos graxos livres no óleo de soja bruto em relação aos outros óleos dentro de cada marca podem estar relacionados com a produção de soja, pois o Brasil é um dos maiores produtores desta oleaginosa e, consequentemente, o tempo de armazenamento do grão é inferior às demais matérias-primas utilizadas para a produção de óleos. E, ainda, a refinação na indústria é em maior quantidade para o óleo de soja, e com isso, o tempo de armazenamento do óleo bruto torna-se inferior.
O valor máximo permitido de ácidos graxos livres pelo Codex Alimentarius Commission (2009) para óleos brutos é de 2,0% em ácido oleico. Assim, os óleos vegetais brutos, exceto de canola marcas M4 e M5; milho marcas M2, M4 e M5; e girassol marca M2, apresentaram resultados satisfatórios quanto aos teores de ácidos graxos livres.
Ao comparar o índice de peróxidos entre as marcas, o maior índice encontrado para o óleo de soja foi a marca M5 (6,2 meq O2/kg), conforme Tabela 2. Para o óleo de canola, os menores índices foram para as marcas M1 e M4. No óleo de milho houve variação de 0,8 a 6,1 meq O2/kg, e para o óleo de girassol, os índices entre as marcas variaram significativamente (p ≤ 0,05), alcançando valores próximos de 15 meq O2/kg.
Entre os tipos de óleos para a mesma marca, o óleo de girassol apresentou maior índice de peróxidos, exceto para a marca M2, onde observou-se que o maior índice foi para o óleo de milho (6,1 meq O2/kg). Os índices de peróxidos obtidos para o óleo de soja bruto foram superiores ao valor de 1,89 meq/kg encontrado por Farhoosh e Tavassoli-Kafrani (2010), enquanto para o óleo de canola bruto, os índices foram inferiores ao encontrado por Ghazani, García-Lattas e Marangoni (2013) que obtiveram 6,8 meq O2/kg, e superiores a 1,94 meq O2/kg, conforme Farhoosh e Tavassoli-Kafrani (2010).
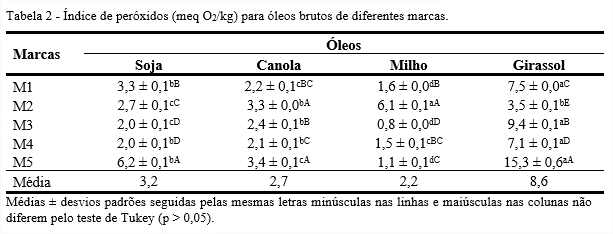
Os peróxidos são formados devido à intervenção de um radical que reage com o ácido graxo insaturado, que, em presença do oxigênio molecular, reagem e são convertidos em outros radicais formando os peróxidos. Considerados como produtos primários da oxidação, os peróxidos podem remover um átomo de hidrogênio de outra cadeia graxa levando à formação de hidroperóxido e outro radical graxo (SOLOMONS; FRYHLE, 2009).
Elevados valores de índice de peróxidos encontrados nos óleos brutos, principalmente de girassol, indicam que, de alguma forma, o óleo foi exposto a processo oxidativo, o que pode ter ocorrido durante o preparo da matéria-prima, extração ou armazenamento do óleo (CASTELO-BRANCO; TORRES, 2011).
A legislação brasileira (BRASIL, 2021) e o Codex Alimentarius Commission (2009) estabelecem limite máximo de 15 meq O2/kg para óleos vegetais brutos. Os valores médios do índice de peróxidos para os óleos brutos estão de acordo com os limites estabelecidos, com exceção do óleo de girassol bruto, marca M5, que ficou pouco acima do limite especificado. Das cinco marcas analisadas, o óleo de milho obteve menores índices de peróxidos em quatro marcas, divergindo apenas na marca M2, cujo menor índice foi para o óleo de soja.
O valor de p-anisidina é uma medida da quantidade de α e β aldeídos, apesar de ser mais sensível para os aldeídos insaturados do que para os aldeídos saturados, porque os produtos coloridos formados pelos aldeídos insanturados absorvem mais fortemente no comprimento de onda de 350 nm. Este teste é usado para determinar a qualidade dos óleos, a eficiência do processamento e as alterações durante a estocagem (GUIOTTO et al., 2014).
Dentre as marcas avaliadas, observa-se que houve variação significativa para as marcas do óleo de soja (p ≤ 0,05). Isto indica os diferentes status oxidativos para estes óleos (Tabela 3).
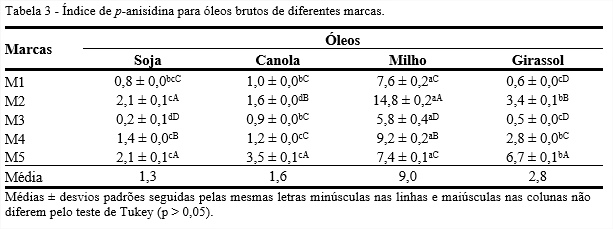
Entre os tipos de óleos, o de soja apresentou menor índice de p-anisidina na marca M3 e o de girassol nas marcas M1 e M3. Os maiores índices foram observados para o óleo de milho em todas as marcas avaliadas, tendo como maior média, a marca M2. Altos índices de anisidina podem estar associados a elevados índices de peróxidos.
A formação de produtos da oxidação secundária aumenta durante a estocagem dos óleos, o que pode estar relacionado à presença de umidade, que varia de 300 a 900 mg/kg em óleos vegetais, e consequente variação nos valores de p-anisidina (KIM; KIM; LEE, 2014). Baseado nos dados obtidos, de maneira geral, os óleos de soja e canola apresentaram menores quantidades de α e β aldeídos.
De acordo com Shahidi (2005), os óleos brutos podem ter índice de p-anisidina de 1 a 3. Neste estudo, 60% das amostras analisadas encontram-se abaixo de 3. Na legislação brasileira, não há limites industriais/comerciais de índices de p-inisidina para óleos brutos (BRASIL, 2021). A confirmação ou não da oxidação lipídica pode ser demostrada pelo valor totox, que é obtida por uma equação que relaciona o valor de índice de peróxidos e o valor de p-anisidina (Tabela 4).
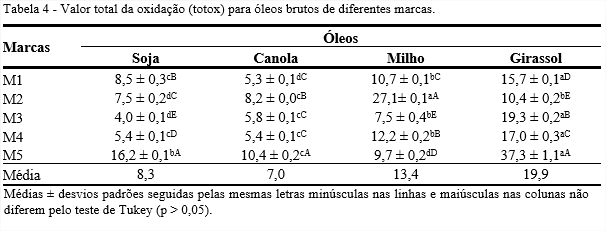
Observa-se que houve diferença significativa entre todas as marcas para os óleos de soja, milho e girassol (p ≤ 0,05). A marca M5 foi a que apresentou maiores valores de totox em óleos brutos, exceto para o óleo de milho. Entre os tipos de óleos, o de girassol, apresentou elevados valores de totox, seguido do óleo de milho, marca M2. Uma vez que o valor totox está associado ao índice de peróxidos e ao valor de p-anisidina, a variação entre os valores para as marcas e tipos de óleos, deve-se a diferentes valores obtidos para estes índices em cada análise.
Os valores totox encontrados para o óleo de soja bruto marcas M2, M3 e M4 foram inferiores a 8,1, obtido por Bachari-Saleh et al. (2013). Em óleo de canola, Ghazani, García-Lattas e Marangoni (2013) obtiveram 16,4 de totox, sendo este valor superior aos encontrados neste estudo para todas as marcas de óleo de canola bruto. Elevados valores podem gerar dificuldade durante a refinação e indicam a oxidação lipídica, o que pode influenciar na estabilidade oxidativa de óleos.
A partir dos dados obtidos nas análises supracitadas, observa-se que as indústrias carecem de ajustes de processos, principalmente em relação à obtenção de óleos brutos de girassol e milho. Pode-se citar dentre estes, ajustes na secagem, armazenamento adequado dos grãos e sementes e controle dos parâmetros de extração do óleo. Tudo isso pode interferir tanto no índice de peróxidos, quanto no valor de p-anisidina, influenciando, assim, o valor totox utilizado para avaliar a oxidação total.
A extinção específica fornece informações sobre a qualidade de um óleo, seu estado de conservação e alterações causadas pelo processamento. Das marcas analisadas para o mesmo tipo de óleo, observa-se que não houve diferença significativa entre as marcas M1 e M2; M1 e M3 para o óleo de soja (Tabela 5). A marca M3 apresentou os menores valores de extinção específica para os óleos de canola, milho e girassol. A marca M2 apresentou maior valor de extinção para os óleos de milho e girassol.
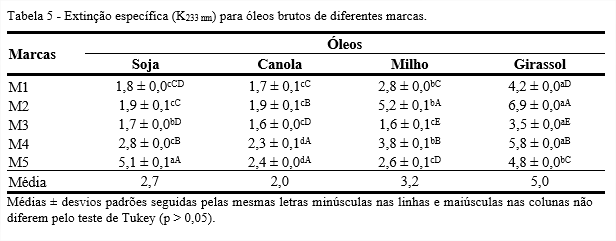
Para os diferentes tipos de óleos, observa-se que, em média, o óleo de girassol apresentou maiores valores de extinção específica, o que pode estar relacionado à presença de maior quantidade de ácido linoleico, o que faz com que o óleo se torne mais susceptível à oxidação lipídica. As variações encontradas entre o mesmo tipo de óleo e nas diferentes marcas podem estar relacionadas à composição dos ácidos graxos de cada óleo, pois, se os parâmetros de extração e armazenamento dos óleos brutos não forem devidamente respeitados, o teor de ácidos graxos poli-insaturados presentes no óleo estará diretamente relacionado ao valor de dienos conjugados (SHAHIDI, 2005).
Analisando os óleos brutos, observa-se que independentemente do tipo de óleo, houve variação entre as marcas para os valores de extinção específica K270 nm, conforme Tabela 6. Em geral, baixos valores de trienos conjugados estão relacionados com matéria-prima de boa qualidade.
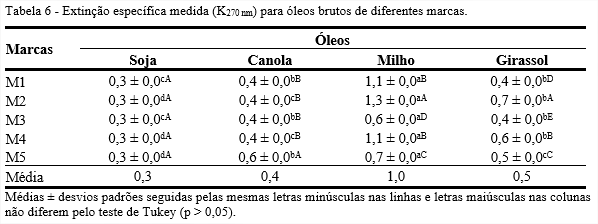
A extinção específica em 270 nm reflete a formação dos trienos conjugados e de compostos secundários durante o processo de oxidação, que é proporcional à absorção de oxigênio no óleo. Dos resultados entre as marcas, a M3 apresentou menores valores de trienos conjugados, indicando que o processo oxidativo foi menor para esta marca. Em relação ao tipo de óleo, o de soja apresentou, em média, 0,3 desse composto, enquanto o óleo de milho teve, em média, 1,0.
Houve diferença significativa entre as marcas analisadas para a matéria insaponificável (Tabela 7), e a marca M4 foi a que apresentou os menores percentuais de matéria insaponificável para os óleos de soja, canola e girassol. Entre os tipos de óleos, o de soja apresentou os menores teores (0,6-1,3%), enquanto o de milho apresentou os maiores (2,1-2,8%).
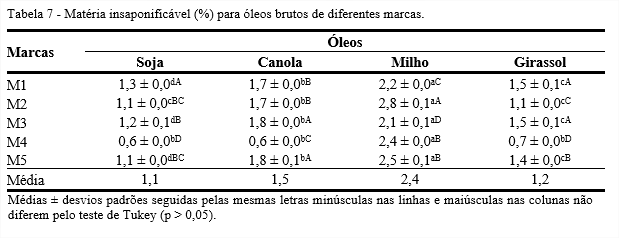
Em geral, os óleos possuem pequenas quantidades de matéria insaponificável, que consiste de tocoferóis, fitosteróis, carotenoides, compostos fenólicos, hidrocarbonetos, bem como pigmentos e minerais que também podem estar presentes (SHAHIDI, 2005; SINGH, 2013). Estes componentes variam nos diferentes tipos de óleos e suas proporções dependem da matéria-prima inicial.
O Codex Alimentarius Commission (2009) estabelece limites de matéria insaponificável de: ≤ 1,5% para óleo de soja; ≤ 2,0% para óleo de canola; ≤ 2,8% para óleo de milho; ≤ 1,5% para óleo de girassol. Excetuando o óleo de milho bruto da marca M2, todos os óleos vegetais avaliados neste estudo estão dentro dos níveis estabelecidos pela legislação. A matéria insaponificável em óleo de milho, tanto bruto como refinado, é maior que em outros óleos, pois cerca de 60% desta matéria é composta de esteróis e a maioria se encontra esterificada aos ácidos graxos (JORGE, 2009).
O índice de estabilidade oxidativa é a medida da resistência dos lipídios à oxidação, que é influenciada por fatores tais como a temperatura e concentração de componentes minoritários entre outros.
A estabilidade oxidativa dos óleos brutos variou de 4,4 a 26,9 h para óleo de soja, de 10 a 10,9 h para óleo de canola, de 2,9 a 22,8 h para óleo de milho e de 1,7 a 5,4 h para óleo de girassol (Tabela 8). Os óleos brutos, em geral, possuem elevada estabilidade, pois possuem maiores quantidades de antioxidantes naturais (TAYLOR, 2005).
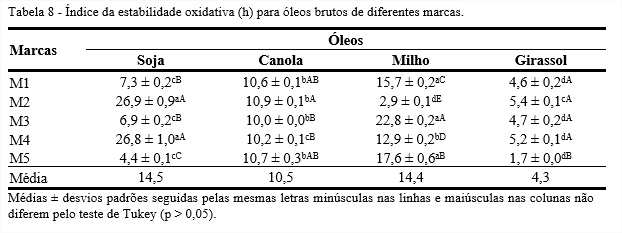
Entretanto, para o óleo de soja marca M5, observa-se baixa estabilidade oxidativa, assim como para os óleos de milho marca M2 e óleo de girassol marca M5. Tal fato pode estar associado à degradação oxidativa, pois, estes óleos apresentaram altos valores totox. Baixos valores de estabilidade oxidativa podem ainda estar relacionados à presença de metais nos óleos, principalmente íons de cobre e ferro, e à presença de fósforo, que são conhecidos por serem pró-oxidantes eficazes na oxidação lipídica e agirem acelerando a deterioração do óleo (BREVEDAN; CARELLI; CRAPISTE, 2000).
Pode-se inferir que as menores estabilidades oxidativas para o óleo de girassol quando comparadas com as estabilidades dos demais óleos estudados, ocorrem devido à baixa ou inexistência de teores de γ- e δ-tocoferóis (TASAN; DEMIRCI, 2005). Além disso, a presença do ácido graxo linoleico, que é altamente susceptível à oxidação, provoca aumento da velocidade da reação de oxidação diminuindo a estabilidade oxidativa desse óleo.
Nos óleos brutos estudados, destacam-se com alta estabilidade oxidativa o de soja, marcas M2 e M4, seguido do óleo de milho, marca M3, cuja elevada estabilidade pode estar relacionada aos compostos fenólicos presentes nestas amostras. Observa-se que o óleo de milho, em geral, apresentou estabilidade superior a 12 h, exceto para a marca M2. Este fato pode estar relacionado ao maior teor de matéria insaponificável neste óleo, em relação aos demais óleos.
A estabilidade oxidativa do óleo de milho bruto foi superior à encontrada por Dolde e Wang (2011) que obtiveram 11,57 h, exceto para a marca M2, nas mesmas condições de análises deste estudo. Para o óleo de girassol bruto, a estabilidade oxidativa média foi inferior ao resultado encontrado por Lamas, Crapiste e Constenla (2014) que obtiveram 17,25 h.
Além da composição em ácidos graxos, outros fatores como a posição destes na molécula de triacilglicerol; a presença e composição de tocoferóis, carotenoides, esteróis; o tipo de matéria-prima; a concentração de compostos secundários com características antioxidantes ou pró-oxidantes e as condições de processamento e de armazenamento podem influenciar sobre a estabilidade oxidativa dos óleos (MERRILL et al., 2008).
CONCLUSÕES
Independentemente das marcas estudadas, considerando as médias gerais para os diferentes óleos brutos, pode-se apontar que o óleo de soja apresentou melhor qualidade do ponto de vista dos ácidos graxos livres, índice de p-anisidina e K270 nm.
Os óleos de soja e milho exibiram maiores índices de estabilidade oxidativa (14 h), enquanto o óleo de milho obteve maior quantidade de matéria insaponificável que os demais, ambos os parâmetros são desejáveis em óleos vegetais.
De acordo com os resultados obtidos das análises físico-químicas, os óleos brutos podem ser considerados, em geral, de boa qualidade.
AGRADECIMENTOS
Agradecimentos à Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), pela concessão da bolsa de doutorado, e ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), pela bolsa de Produtividade em Pesquisa.
REFERÊNCIAS
AOCS. AMERICAN OIL CHEMISTS’ SOCIETY. Oficial Methods and Recommended Practices of the American Oil Chemists’ Society. 6 ed. Champaign: AOCS, 2009.
BACHARI-SALEH, Z.; EZZATPANAH, H.; AMINAFSHAR, M.; SAFAFAR, H. J. The effect of refining process on the conjugated dienes in soybean oil.Journal of Agricultural Science and Technology, Teherán, v. 15, n. 6, p. 1185-1193, 2013.
BRASIL. Agência Nacional de Vigilância Sanitária. Instrução Normativa nº 87, de 15 de março de 2021. Estabelece a lista de espécies vegetais autorizadas, as designações, a composição de ácidos graxos e os valores máximos de acidez e de índice de peróxidos para óleos e gorduras vegetais, Brasília, DF, ANVISA, 2021.
BREVEDAN, M. I. V.; CARELLI, A. A.; CRAPISTE, G. H. Changes in composition and quality of sunflower oils during extraction and degumming. Grasas y Aceites, Sevilla, v. 51, p. 417-423, 2000.
CASTELO-BRANCO, V. N.; TORRES, A. G. Capacidade antioxidante total de óleos vegetais comestíveis: determinantes químicos e sua relação com a qualidade dos óleos. Revista da Nutrição, Campinas, v. 24, n. 1, p. 173-187, 2011.
CHEW, S. C.; ALI, M.A. Recent advances in ultrasound technology applications of vegetable oil refing. Trends in Food Science & Technology, Cambridge, v. 116, p. 468-479, 2021.
CODEX ALIMENTARIUS COMISSION (FAO/WHO). Codex standart for named vegetable oils: codex stan 210-1999. Codex Alimentarius, v. 10, 2009.
DOLDE, D.; WANG, T. Oxidation of crude corn with and without elevated trocotrienols.Journal of the American Oil Chemists’ Society, Chicago,v. 88, n. 9, p.1367-1372, 2011.
FARHOOSH, R.; TAVASSOLI-KAFRANI, M. H. Polar compounds distribution of sunflower oil as affected by unsaponifiable matters of Bene hull oil (BHO) and tertiary-butylhydroquinone (TBHQ) during deep-frying. Food Chemistry, Filadelfia, v. 122, n. 1, p. 381-385, 2010.
GHAZANI, S. M.; GARCÍA-LLATAS, G.; MARANGONI, A. G. Minor constituents in canola oil processed by traditional and minimal refining methods. Journal of the American Oil Chemists’ Society, Chicago, v. 90, n. 5, p. 743-756, 2013.
GUIOTTO, E.; IXTAINA, V.Y.; NOLASCO, S. M.; TOMÁS, M.C. Effect of storage conditions and antioxidants on the oxidative stability of sunflower–chia oil blends. Journal of the American Oil Chemists’ Society, Chicago, v. 91, n. 5, p. 767-776, 2014.
HUI, Y. H. Bailey’s industrial oil and fat products: processing technology. New York: Wiley Interscience Publication, 5. Ed., 1996, vol. 4. 600 p.
JORGE, N. Química e tecnologia de óleos vegetais. São Paulo: Cultura Acadêmica, 2009. 165 p.
KIM, J.; KIM, M.; LEE, J. Effects of deuterium oxide on the oxidative stability and change of headspace volatiles of corn oil. Journal of the American Oil Chemists’ Society, Chicago, v. 91, n. 4, p. 623-628, 2014.
LAMAS, D. L.; CRAPISTE, G. H.; CONSTENLA, D. T. Changes in quality and composition of sunflower oil during enzymatic degumming process. LWT – Food Science and Technology, London, v. 58, p. 71-76, 2014.
MERRILL, L.; PIKE, O. A.; OGDEN, L. V.; DUNN, M. L. Oxidative stability of conventional and high-oleic vegetable oils with added antioxidants. Journal of the American Oil Chemists’ Society, Chicago, v. 85, n. 8, p. 771-776, 2008.
OSAWA, C. C.; GONÇALVES, L. A. G.; RAGAZZI, S. Titulação potenciométrica aplicada na determinação de ácidos graxos livres de óleos e gorduras comestíveis. Química Nova, São Paulo, v. 29, n. 3, p. 593-599, 2006.
PRZYBYLSKI, R.; MAG, T.; ESKIN, N. A. M.; McDONALD, B. E. Canola oil. In: SHAHIDI, F. Bailey’s industrial oil and fat products. 6. ed. Wiley: Hoboken, 2005. v. 2. Cap. 2, p. 61-122.
SHAHIDI, F. Quality Assurance of fats and oils. In: SHAHIDI, F. Bailey’s Industrial Oil Fat Products. 6 ed., v. 1, Newfoundland: John Wiley & Sons, 2005. Cap. 14, p.565-576.
SINGH, A. Sitosterol as an antioxidant infrying oils. Food Chemistry, Filadelfia, v. 137, n. 1-4, p. 62-67, 2013.
SOLOMONS, T. W. G.; FRYHLE, C. B.; Química Orgânica. Rio de Janeiro, v. 1. Editora: GEN/LTC, 2009.
SULIMAN, T. E. M. A; JIANG, J.; LIU, Y. Chemical refining of sunflower oil: effect on oil stability, total tocopherol, free fatty acids and colour. International Journal of Engineering Science and Technology, Indore, v. 5, n. 2, p. 449-454, 2013.
TASAN, M.; DEMIRCI, M. Total and individual tocopherol contents of sunflower oil at different steps of refining. European Food Research Technology, New York, v. 220, n. 3-4, p. 251-254, 2005.
TAYLOR, D. R. Bleaching. In: “Bailey’s Industrial Oil and Fat Products”, (Ed.)” Shahidi, F. John Wiley and Sons Publication, Hoboken, NJ, 2005. v. 2, pp. 285-339.
USDA – UNITED STATES DEPARTMENT OF AGRICULTURE – Disponível em: https://apps.fas.usda.gov/psdonline/circulars/oilseeds.pdf. Acesso em: 2 fev 2022. WANASUNDARA, U. N.; SHAHIDI, F. Canola extract as an alternative natural antioxidant for canola oil. Journal of the American Oil Chemists’ Society, Champaign, v. 71, p. 817-822, 1994.