OTIMIZAÇÃO DA EXTRAÇÃO ASSISTIDA POR ULTRASSOM DE COMPOSTOS FENÓLICOS DO RESÍDUO DA PRODUÇÃO DE VINHO
Capítulo de livro publicado no livro do VIII ENAG E CITAG. Para acessa-lo clique aqui.
DOI: https://doi.org/10.53934/9786585062046-65
Este trabalho foi escrito por:
Letícia R. Bohn; Guilherme M. Mibielli ; Joel G. Teleken*
*Autor correspondente (Corresponding author) – Email: [email protected]
Resumo: O bagaço de uva é um subproduto abundante da indústria do vinho que consiste no resto das cascas, suco resdidual, sementes e engasgos. Estima-se que este resíduo represente cerca de 30% do peso total da uva utilizada no processo de vinificação. Considerando que tais resíduos são ricos em compostos bioativos, amplamente reconhecidos por suas propriedades promotoras de saúde e aplicações tecnológicas, a extração dessas substâncias representa uma alternativa para a obtenção de produtos de alto valor agregado que podem ser utilizados como ingredientes nas indústrias alimentícia, cosmética e farmacêutica. Dessa forma, este estudo visa otimizar o processo de obtenção de compostos fenólicos a partir de resíduos de vinificação por meio de extração assistida por ultrassom. Para otimização do processo realizou-se um DCCR tendo como variáveis: temperatura, razão sólido-líquido, potência de ultrassom e concentração de etanol. Os resultados variaram de 11,81 a 51,21 mg/g biomassa seca, tendo a razão sólido/líquido como variável significa negativa. A partir destes resultados, a 95% de confiança, o modelo matemático codificado de segunda ordem para a extração de compostos fenólicos foi validado estatisticamente e experimentalmente. Os melhores resultados em termos de CFT foram também avaliados quanto ao seu perfil fenólico por HPLC-MS, tendo ácido siríngico como composto mais abundante (41,8 mg/L).
Palavras–chave: Bagaço de uva; Extração etanólica; Reaproveitamento de coprodutos
Abstract: Grape pomace is an abundant by-product of the wine industry that consists of the rest of the skins, residual juice, seeds and stalks. It is estimated that this residue represents about 30% of the total weight of the grape used in the winemaking process. Considering that such residues are rich in bioactive compounds, widely recognized for their health-promoting properties and technological applications, the extraction of these substances represents an alternative for obtaining products with high added value that can be used as ingredients in the food, cosmetic and pharmaceutical industries. Thus, this study aims to optimize the process of obtaining phenolic compounds from winemaking residues through ultrasound-assisted extraction. To optimize the process, a DCCR was performed with the following variables: temperature, solid-liquid ratio, ultrasound power and ethanol concentration. The results ranged from 11.81 to 51.21 mg/g dry biomass, with the solid/liquid ratio as a variable meaning negative. From these results, at 95% confidence, the second-order coded mathematical model for the extraction of phenolic compounds was statistically and experimentally validated. The best results in terms of TFC were also evaluated for their phenolic profile by HPLC-MS, with syringic acid as the most abundant compound (41.8 mg/L).
Keywords: By-products reuse; Ethanolic extraction; Phenolic compounds
INTRODUÇÃO
O Brasil é o 18º maior produtor de vinho do mundo, tendo registrado em 2020 uma produção de 430 milhões de litros, fruto da ampliação das áreas de cultivo de uvas e agroindústrias de vinhos nas últimas décadas. O vinho se tornou a bebida da pandemia aumentando sua base de consumidores no Brasil para 51 milhões de pessoas, com uma estimativa de aumento ainda maior neste número para o ano de 2022. Além disso, com a geada nos vinhedos da Europa, os preços para importação aumentaram mais de 20% no final de 2021, o que reforça a estimativa de aumento de produção para o ano de 2022 (1).
O processamento da uva na indústria vinícola resulta na produção de resíduos, tanto sólidos, quanto líquidos. O bagaço é o principal subproduto gerado, o qual é separado durante as etapas de esmagamento e prensagem das uvas, estima-se uma geração de 20 a 30 % (m/m) desse resíduo em relação ao peso inicial de uva utilizada no processo (2). O aumento registrado e esperado para produção de vinho corresponde também a um aumento na quantidade de resíduos sólidos gerados, que em sua maioria, são utilizados para adubação do solo nas próprias vinícolas ou para alimentação animal. Porém, a destinação irregular desses resíduos sólidos de forma inadequada pode provocar poluição ambiental, uma vez que liberam quantidades significativas de efluentes líquidos, os quais contém alto teor de nutrientes, matéria orgânica e outros elementos que podem alterar o ambiente, tanto o solo como a água (3).
Considerando que os resíduos da vinicultura são ricos em compostos bioativos, uma vez que a maior parte dos polifenóis da uva provém das partes sólidas da uva (pele e sementes), esses resíduos são uma fonte importante para obtenção de outros produtos de interesse industrial. O produto pioneiro e mais tradicional da utilização do bagaço de uva é o óleo de semente, que no Brasil ainda tem uma produção muito pequena, porém é o coproduto mais valorizado dos resíduos da cadeia da uva até o momento, sendo utilizado principalmente como cosmético (4). A utilização de outras frações de resíduos ainda é limitada, demonstrando o potencial existente para agregar valor a este material.
Para ter acesso aos componentes bioativos oriundos da matéria-prima vegetal utilizam-se métodos de extração. A escolha do método para extrair estes componentes depende da estabilidade térmica e natureza dos compostos a serem analisados. Dentre os diversos métodos para a obtenção de compostos bioativos presentes em matrizes vegetais, o uso de ultrassom e o emprego de líquidos pressurizados vem emergindo como abordagens potenciais, visando à máxima recuperação destes compostos aliada à alta estabilidade e baixo custo energético
Frente ao exposto, a presente proposta visa otimizar a extração de compostos fenólicos por meio de ultrassom, caracterizando os extratos quanto à sua composição em termos de compostos fenólicos totais. Dessa forma, buscando fontes alternativas de aproveitamento desse resíduo que possa agrupar características desejáveis na formulação de novos produtos da indústria alimentícia, química e farmacêutica.
MATERIAL E MÉTODOS
O bagaço de uva proveniente da produção de vinho tinto foi fornecido pela vinícola Cantina do Tônico, localizada no município de Palmitos -SC. O material é composto de cascas, sementes, engasgos e suco remanescente da uva bordô (Vitis labrusca) utilizadas na produção do vinho
Após a coleta, as amostras foram submetidas a tratamento térmico para inativação enzimática, esse processo deu-se em banho maria por um período de 15 min, o qual foi contabilizado a partir do momento que as amostras atingiram a temperatura de 70°C. Posteriormente, o material foi seco em estufa de ar circulante, a temperatura de 50°C por 72 horas. Após a secagem percebeu-se que a maior parte das sementes da uva separaram-se do restante do material. Uma vez que o óleo da semente de uva é o coproduto mais valorizado, tendo sua produção bem definida (4); optou-se por separar a maior parte das sementes e trabalhar com o restante do material (casca, engasgos, suco residual e algumas sementes). Em seguida o material foi moído em um moinho de facas até partículas inferiores a 0,6 mm e armazenado em temperatura de congelamento (-18 °C), em bolsas hermeticamente fechadas, envolvidas com papel laminado para proteger da luz.
A fim de conhecer a biomassa que será utilizada como matéria prima no processo de extração de compostos fenólicos, foi realizada a caracterização da biomassa quanto a sua umidade e distribuição granulométrica seguindo o procedimento padrão NREL (Nacional Renewable Energy Laboratory) descrito por Sluiter et. al. (5). A umidade e a distribuição granulométrica foram determinadas uma vez que esses fatores podem influenciar a eficiência do processo de extração (6).
A extração de compostos fenólicos do resíduo da produção de vinho foi realizada em banho de ultrassom. A matéria prima foi aferida em tubo de ensaio com rosca e em seguida, adicionado à solução de extração. Foi utilizado água destilada e etanol 95% como líquidos extratores com o intuito de proporcionar o aproveitamento da metodologia, objetivando extratos que poderão ser usados em formulações alimentícias, cosméticas e farmacêuticas. Decorrido o tempo de extração, as amostras foram centrifugadas por 5 minutos, na temperatura de 25 °C a 5000 rpm. Em seguida, foi desprezado o resíduo, e o extrato (sobrenadante) foi armazenado em tubos de Falcon envolto em papel alumínio no freezer (-18 °C) até o momento da realização das análises.
Inicialmente experimentos preliminares foram realizados para avaliar a influência do tempo de extração dos compostos de interesse. Para tanto as demais condições de extração foram fixadas em: razão sólido-líquido de 20 g/L, ou seja, 0,2 g de amostra foram submetidas à extração em um volume fixo de 10 mL de uma solução de EtOH:H2O (50:50, v:v), em intervalos de 15 minutos, até o tempo de 120 min. Os parâmetros, potência de ultrassom e temperatura foram fixados em 100% e 50°C respectivamente nos ensaios preliminares. A escolha destes parâmetros se deu em função de obter-se uma tecnologia extrativa rápida e com gasto mínimo de energia e de solvente orgânico, tendo-seuma temperatura inferior à temperatura de degradação de alguns compostos fenólicos, o que ocorre a partir de 70 °C (7).
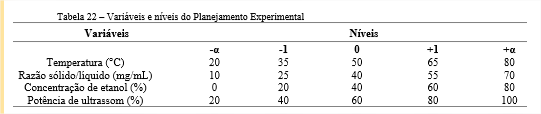
A otimização do processo de obtenção do extrato foi realizada com o auxílio de um planejamento de experimentos. A técnica foi empregada objetivando compreender a influência das variáveis estudadas e encontrar a melhor condição de extração do processo. Para tanto, foi realizado um DCCR utilizando os pontos axiais, a fim de se avaliar o efeito quadrático das variáveis investigadas. O delineamento realizado foi um fatorial completo 24, composto por quatro variáveis, dois níveis, pontos axiais e pontos centrais. Salienta-se que todos os ensaios foram realizados em triplicata e em ordem randômica. A Tabela 1 apresenta as variáveis e níveis do DCCR.
Os extratos obtidos foram caracterizados quando ao teor de compostos fenólicos totais através do método espectrofotométrico pelo reagente de Folin-Ciocalteau, conforme a metodologia descrita por Carniel et. al. (8). Os extratos que apresentaram melhores condições de compostos fenólicos totais foram subtidos a análise do perfil fenólico utilizando um cromatógrafo líquido Shimadzu acoplado ao detector de massa (HPLC-MS) com fonte de ionização por eletrospray (ESI (-)) seguindo a metodologia descrita por Arruda et. al. (9). As análises estatísticas foram realizadas utilizando o software Protimiza®, executando análise de variância e o teste de comparação das médias pelo teste de Tukey com ɑ = 5%.
RESULTADOS E DISCUSSÃO
A Figura 1 apresenta a distribuição granulométrica da biomassa a qual foi realizada por peneiras na Série de Taylor com abertura de 9 (2mm), 16 (1mm), 30 (0,6mm), 60 (0,297mm), 100 (0,15mm) e fundo (0 mm).
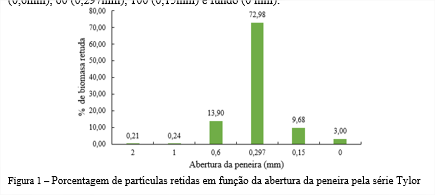
De acordo com a análise granulométrica constatou-se que a biomassa apresenta, em maioria, diâmetros menores a 0,6 mm. Visto que partículas de menores tamanho favorecem o processo de extração dos compostos fenólicos, uma vez que essas apresentam maior área superficial, facilitando o processo de transferência de massa (10), reservou-se o material retido nas peneiras de 60 e 100 mesh, juntamente com o material de fundo para ser utilizada nos demais experimentos.
Em relação do teor de umidade da biomassa, a Tabela 2 apresenta os teores de umidade do material logo após ser coletado (Biomassa 1) e do material após a secagem e redução do tamanho das partículas em moinho (Biomassa 2).

Ao ser coletada a biomassa possuía significativa quantidade de suco remanescente do processo de fermentação, o que justifica o alto teor de umidade (71,28%). A determinação de umidade é importante, pois o bagaço de uva é altamente perecível, devido ao elevado teor de umidade e à atividade da água (11). Após o processo de secagem em estufa a biomassa permaneceu apenas com 10,17% de umidade, tornando-se estável ao armazenamento (11).
Na tabela 3 são apresentados os resultados em termos de compostos fenólicos totais da cinética inicial realizada para avaliar a influência do tempo nas extrações. Os resultados estão expressos como mg de Ácido Gálico equivalente por grama de biomassa seca.
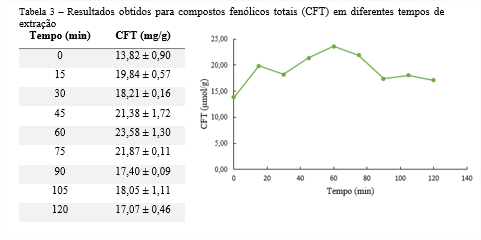
A realização da cinética de extração é uma etapa importante para otimização do processo visto que curtos períodos de extração podem não ser suficientes para a completa transferência dos solutos para a fase orgânica. Por outro lado, longos tempos de extração em elevadas temperaturas podem oxidar os compostos fenólicos da amostra. Conforme pode ser visualizado na Tabela 3, o ensaio de 60 minutos foi o de maior rendimento na extração (23,58 mg/g). A partir de 60 minutos a extração se estabiliza e em tempos mais prologando ocorre uma redução nos resultados em termos de CFT.
Dessa forma, determinou-se a realização dos ensaios do planejamento experimental para otimização da extração com o tempo fixado em 60 minutos. Na tabela 4 são apresentados os resultados em termos de compostos fenólicos totais, expressos como mg de Ácido Gálico equivalente por g de biomassa seca, do planejamento experimental.
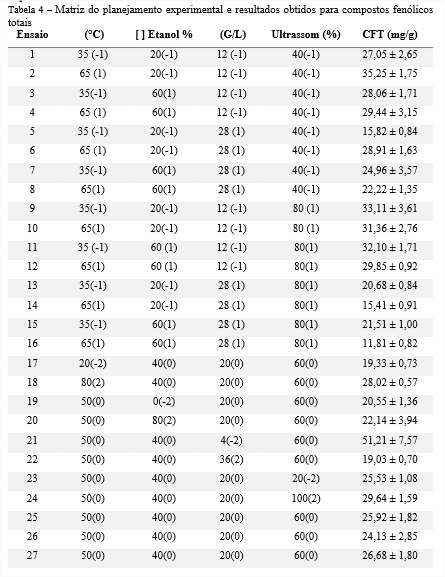
Avaliando os resultados da Tabela 4, para compostos fenólicos totais, verificou-se que os resultados variaram de 11,81 a 51,21 mg/g biomassa seca. Braga et. al. (12) a partir do bagaço de uva liofilizado, em banho ultrassônico à temperatura ambiente por 15 minutos, utilizando etanol 80% obteve 60,28 mg/g biomassa seca. Enquanto que Rockenbach et. al. (13) sob agitação mecânica durante 2 horas, utilizando acetona como solvente 50 e 70% (v/v) obteve nas melhores condições valores entre 65,6 e 79,5 mg/g a partir do bagaço de uva. Llobera e Cañellas (14), a partir do bagaço de uvas tintas variedade “Manto Negro” (Vitis vinifera), obtiveram teores médios de compostos fenólicos extraídos sequencialmente com metanol a 50% e acetona a 70% (v/v) entre 26,3 e 116,0 mg/g em peso seco.
Diferentes preparos da matéria prima e diferentes métodos e extrativos podem ser os responsáveis pela diferencia dos rendimentos obtidos nesse trabalho e dos reportados na literatura. Contudo, vale destacar que para o trabalho em questão as sementes foram retiradas do bagaço de uva, o que proporciona características diferentes a matéria prima utilizada para extração. Ainda se ressalta que encontrar um método único de extração que seja adequado para a análise de um grupo diverso de fenólicos é complexo devido à diversidade das estruturas químicas e variação de sensibilidade dos compostos às condições de extração (15).
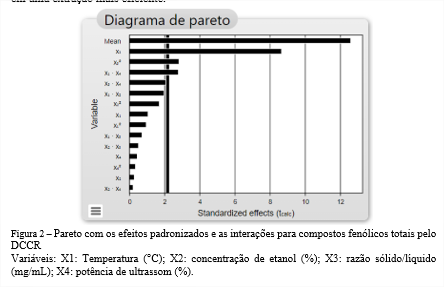
Para esse estudo de otimização, analisando a Figura 2, observa-se que das 4 variáveis estudadas no DCCR apenas a razão sólido/líquido demostrou a 95% de confiança, significância para a extração de compostos fenólicos totais. A diminuição na razão sólido/líquido representa em um aumento no rendimento em termos de CFT. Tal condição pode ser explicada uma vez que quanto maior a quantidade de solução extratora, maior o gradiente de concentração entre a matéria prima e a solução, resultando, portanto, em uma extração mais eficiente.
No estudo de Gruz et. al. (16), para extração com bagaço de uva, a razão solvente/substrato e a temperatura foram parâmetros estatisticamente significativos para todas as variáveis de resposta avaliadas. Sendo que o aumento da temperatura atuou mais fortemente que a razão solvente/substrato. O aumento do teor de etanol também favoreceu a extração dos compostos fenólicos totais.
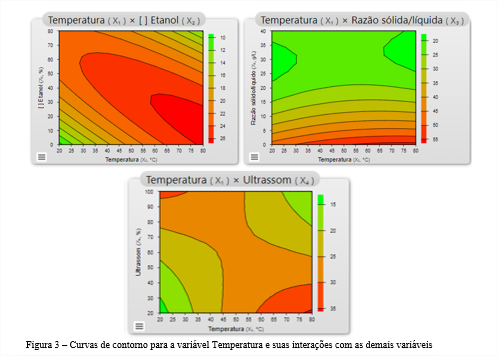
Para esse estudo a temperatura não demostrou efeito significativo, contudo, pode-se observar através da Figura 3, que temperaturas mais altas favorecem a extração dos compostos fenólicos. Ainda assim, devido a interação negativa da temperatura com a potência de ultrassom, usando-se altas potência de ultrassom, o modelo estatístico demostrou que temperaturas mais baixas seriam ideais, para esse caso.
Teles et. al. (17) realizou a otimização do processo de extração do bagaço de uva proveniente da produção de espumantes, através de extração etanólica, com adição de ácido cítrico, assistida por ultrassom. Os resultados variaram de 64,85 a 117,32 mg/g. As extrações mais eficientes ocorreram quando foram utilizadas potências de ultrassom mais altas, maiores concentrações de ácido e menor razão sólido/líquido. González-Centeno et. al. (18), também obtiveram maior teor de compostos fenólicos de bagaço de uva com o aumento da potência de ultrassom.
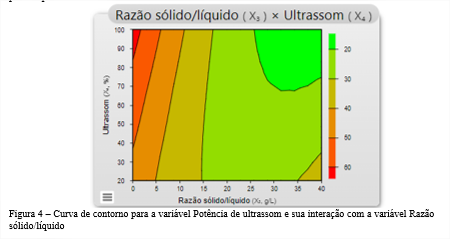
Apesar de a potência de ultrassom não ter se mostrado significativa para esse estudo, através da Figura 4 pode-se observar que o aumento da potência de ultrassom favorece a extração, quando associada a baixas razão sólido/líquido, variável significativa para o processo.
De forma geral, a literatura aponta que, na maioria dos casos, o aumento da temperatura, da razão solvente/substrato e do teor de solvente melhore os processos extrativos. Contudo, as características da matriz e dos compostos de interesse são primordiais para se estabelecer a condição operacional mais favorável do ponto de vista termodinâmico e econômico.
A partir destes resultados, a 95% de confiança, o modelo matemático codificado de segunda ordem para a extração de compostos fenólicos foi validado (Equação 1) pela análise de variância, onde o Fcalc (7,9) foi 4 vezes maior que o Ftab, possibilitando a obtenção de uma superfície de resposta com R²=90,23%.
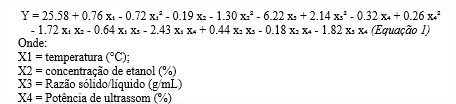
A partir do modelo desenvolvido estaticamente buscou-se uma condição de extração a fim de maximizar a concentração de compostos fenólicos obtidas. Dessa forma de acordo com a equação 1, nas condições de: 65 °C; 40% de etanol; razão sólido/líquido de 4 g/L e potência de ultrassom em 100%, deve-se obter 50,72 mg/g de compostos fenólicos totais. Tal condição foi realizada experimentalmente e obteve-se 51,17±3,65 mg/g de CFT, validando o modelo estatístico experimentalmente.
A fim de se conhecer o perfil fenólico obtido das extrações, as melhores condição em termos de compostos fenólicos totais foram analisadas através de cromatografia líquida acoplada ao detector de massas. Na tabela 5 são apresentados os resultados em termos de compostos fenólicos individuais dos ensaios que apresentaram melhores respostas em termos de compostos fenólicos totais: o ensaio de 60 min na cinética inicial e o ensaio 21 do DCCR; ambos em triplicata. Os resultados estão expressos como mg/L.
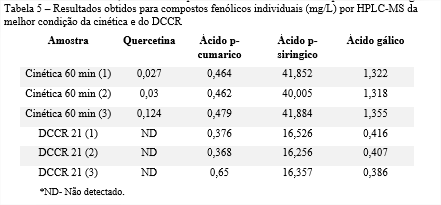
Pode-se observar que os compostos mais presentes no extrato foram os ácidos. Os ácidos fenólicos incluem derivados do ácido benzoico, como o ácido p-cumárico, e cinâmico, como o ácido siringico, sendo os ácidos hidroxicinâmicos a classe mais abundante em subprodutos da indústria do vinho. Outro composto detectado foi a quercetinha, que se trata de um flavonóide, o qual está presente somente na casca da uva, na forma de glicosídeos, os quais possuem importante papel na coloração do vinho, uma vez que, atuam como co-pigmentos (19).
CONCLUSÕES
As questões ambientais são uma preocupação na agricultura e nos processos agroindustriais, sendo a indústria vitivinícola responsável pela geração de grandes quantidades de bagaço de uva, que precisam de uma destinação adequada. A utilização de resíduos de alimentos indústrias como matéria-prima para o desenvolvimento de novos produtos é uma alternativa interessante visto que apresenta custos reduzidos em base operacional e permite o atendimento da legislação ambiental no que se refere a destinação dos resíduos.
O bagaço da uva é rico em compostos fenólicos, os quais podem ser recuperados através de um processo de extração sólido-líquido. O ultrassom mostrou-se uma alternativa promissora para extração de compostos fenólicos totais presentes do resíduo proveniente da indústria da vinicultura, resultando em extratos ricos nesses compostos. As extrações mais eficientes ocorreram com uma menor razão sólido/líquido, 4 g/L, a 50°C, solução de etanol 40% em banho ultrassônico na potência de 60%, durante o período de 60 minutos. No entanto, o desenvolvimento tecnológico para recuperação de compostos bioativos de resíduos agroindustriais deve continuar avançando, a fim de promover uma tecnologia mais eficiente, tanto em termos produtivos como ambientais.
REFERÊNCIAS
- OIV- International Organisation of Vine and Wine. State of the world Vitivinicultural Sector in 2020. 2021.
- Beres C, Costa, G N S, Cabezudo I, Silva-James N K, Teles A S C, Cruz A P G, et al. Towards integral utilization of grape pomace from winemaking process: a review. Waste Management. 2017;68:581-594.
- Botelho V R, Bennemann G D, Torres Y R, Sato A J. Potential for use of the residues of the wine industry in human nutrition and as agricultural input. Grapes and wines: advances in production, processing, analysis and valorization. IntechOpen, 2017.
- EMBRAPA. Tecnologias para o Aproveitamento Integral dos Resíduos da Indústria Vitivinícola. Rio de Janeiro, 2018.
- Sluiter A, Hames B, Ruiz R, Scarlata C, Sluitr J, Templeton D. Determination of Total Solids in Biomass. National Renewable Energy Laboratory (NREL). Golden, 2005.
- Azmir J, Zaidul I S M, Rahman M M, Sharif K M, Mohamed A, Sahena F, et al. Techniques for extraction of bioactive compounds from plant materials: a review. Journal of Food Engineering. 2013;117:426 – 36.
- Machado W M, Pereira A D, Marcon M V. Effect of processing and storage on phenolic compounds present in fruits and vegetables. Exatas. 2012;19:17-31.
- Carniel N, Dallago R M, Dariva C, Bender J P, Nunes A L, Zanella O, et al. Microwave-Assisted Extraction of Phenolic Acids and Flavonoids from
Physalis angulata. Journal of Food Process Engineering. 2017;40:1–11. - Arrud H S. Determination of free, esterified, glycosylated and insoluble-bound phenolics composition in the edible part of araticum fruit (Annona crassiflora Mart.) and its by-products by HPLC-ESI-MS/MS. Food Chemistry. 2018;245:738-749.
- Pereira C G, Meireles M A A. Supercritical fluid extraction of bioactive compounds: fundamentals, applications and economic perspectives. Food and Bioprocess Technology. 2010;3:340-372.
- Goul, A M, Thymiatis K, Kaderides K. Valorization of grape pomace: Drying behavior and ultrasound extraction of phenolics. Food and Bioproducts Processing. 2016;100:132–144.
- Braga G C, Melo P S, Bergamaschi K B, Tiveron A P, Massarioli A P. Extraction yield, antioxidant activity and phenolics from grape, mango and peanut agro-industrial by-products. Ciência Rural. 2016:46(8):1498-1504.
- Rockenbach I I, Silva G L, Rodrigues E, Kuskoski E M, Fett R. Influência do solvente no conteúdo total de polifenóis, antocianinas e atividade antioxidante de extratos de bagaço de uva (Vitis vinifera) variedades Tannat e Ancelota. Ciência e Tecnologia de Alimentos. 2008;28:23-44.
- Llobera A, Cañellas J. Dietary fibre content and antioxidant activity of Manto Negro red grape (Vitis vinifera): pomace and stem. Food Chem. 2007;101:659-666.
- Antolovich M., Prenzler P, Robards K, Ryan D. Sample preparation in the analysis of phenolic compounds in fruits. Analyst. 2000;125: 989–1009.
- Gruz A P, Silva C G, Torres A G, Freitas S P, Cabral L M C. Recovery of bioactive compounds from grape pomace. Rev. Bras. Frutic. 2013;35:1147-1157.
- Mazza K E L, Teles A S C, Caldas T W, Brígida A I S, Borguin R G, Tonon R V. Efeito das condições de processo na extração assistida por ultrassom de fenólicos do bagaço de uva. XXV Congresso Brasileiro de Ciência e Tecnologia de Alimentos, 2016.
- González-Centeno M R, Knoerzer K, Sabarez H, Simal S, Rosselló C, Femenia A. Effect of acoustic frequency and power density on the aqueous ultrasonic-assisted extraction of grape pomace (Vitis vinifera L.) A response surface approach. Ultrasonics sonochemistry. 2014;21(6):2176-2184.
- Teixeira A, Baenas N, Dominguez-Perles R, Barros A, Rosa E, Moreno D A, Garcia-Viguera C. Natural bioactive compounds from winery by-products as health promoters: A review. Int. J. Mol. Sci. 2014;15:15638–15678.
Tag:ENAG