NANOPARTÍCULA DE OURO PARA DETECÇÃO DO ÁCIDO PALMÍTICO
Capítulo de livro publicado no livro do I Congresso Latino-Americano de Segurança de Alimentos. Para acessa-lo clique aqui.
DOI: https://doi.org/10.53934/08082023-08
Este trabalho foi escrito por:
Patrícia Avelar Ribeiro *; Ana Luiza Schuenck Alberice Monteiro ; Renata Carolina Zanetti Lofrano ; Jane Sélia dos Reis Coimbra ; Igor José Boggione Santos
*Autor correspondente_ Email:[email protected]
Resumo: A composição do leite, principalmente o teor de gordura, determina a qualidade e seu valor de mercado, portanto a análise deste teor é fundamental para o setor do laticínio. Além da porcentagem total de gordura, a composição dos ácidos graxos livres pode ser utilizada como indicador de qualidade do leite. O ácido palmítico, é um ácido graxo saturado de maior abundância no leite. Atualmente na indústria, os métodos utilizados para medir o teor de gordura são trabalhosos, perigosos e possuem alta margem de erro. Portanto, faz-se necessário um novo sistema de monitoramento para teor de gordura láctea. Dito isso, apresentamos no presente trabalho, a utilização de nanopartículas de ouro com tamanho de 1,2 ± 0,2 nm para detecção do ácido palmítico. A nanopartícula de ouro foi escolhida devido a sua excelente propriedade óptica e apresentou resultados excelentes nos métodos quantitativos de RGB e espectroscopia. Demonstrando assim, a alta capacidade desta nanopartícula para a produção de um nanosensor sensível colorimétrico para detecção de gordura do leite.
Palavras-chave: ácido graxo, gordura láctea, nanosenor colorimétrico, nanotecnologia
Abstract: The composition of milk, especially the fat content, determines its quality and market value, so the analysis of the compounds is critical for the dairy industry. In addition to the total fat percentage, the composition of free fatty acids can be used as an indicator of milk quality. Palmitic acid is the most abundant saturated fatty acid in milk. Currently in the industry, the methods used to measure fat content are labor-intensive, dangerous and have a high margin of error. Therefore, a new monitoring system for milk fat content is needed. That said, we present in the present work, the use of gold nanoparticles with a size of 1.2 ± 0,2 nm for the detection of palmitic acid. The gold nanoparticle was chosen due to its excellent optical property and showed excellent results in quantitative RGB and spectroscopy methods. Thus, demonstrating the high capability of this nanoparticle for the production of a colorimetric-sensitive nanosensor for milk fat detection.
Keywords: fatty acid; milk fat; colorimetric nanosensor; nanotechnology
INTRODUÇÃO
O leite, produzido nas glândulas mamárias das fêmeas dos mamíferos, é um importante fluido biológico que atende as necessidades específicas dos indivíduos, por se tratar de um alimento altamente nutritivo, fonte de carboidratos, gorduras, minerais e vitaminas (1). Os seres humanos, quando bebês consomem o leite advindo da própria espécie, e quando adquirem uma certa idade, passam a consumir o biofluido de outras espécies, sendo que a produção mundial do leite é ofertada por cinco espécies animais, são elas: vacas (83%), búfalas (13%), cabras (2%), ovelhas (1%) e camelo (0,4%) (2). A indústria de laticínios ocupa, atualmente, um importante lugar no setor agrícola, sendo o Brasil, um dos países mais competitivos nos mercados internacionais e o terceiro maior produtor mundial de leite bovino, com um volume anual de 34 bilhões de litros, portanto, o Brasil é um grande protagonista em negócios agroalimentares (3,4).
A composição do leite é um fator essencial para a qualidade dos produtos lácteos, uma vez que as propriedades do leite estão relacionadas com os compostos encontrados no fluido (5). Diversos fatores podem afetar a composição do leite, como a raça, idade, estágio de lactação, estado de saúde, tipo de alimentação dada ao animal e efeitos sazonais e regionais (1). O leite bovino é composto por macronutrientes: água, carboidratos, lipídeos e proteínas, e micronutrientes, como vitaminas e minerais (2).
Os lipídeos estão presentes no leite nas concentrações de 2,9 a 3,5 %, e são considerados um dos componentes mais importantes, visto que são responsáveis pelas propriedades reológicas e organolépticas dos produtos lácteos, bem como, contribuir para características sensoriais e estabilidade em emulsões (6,7). Dentro do glóbulo de gordura láctea, estão presentes os ácidos graxos em diferentes comprimentos de cadeia, sendo o ácido palmítico (C16:0) encontrado em maior quantidade, representando 22 a 35% dos ácidos graxos totais (8,9). O ácido palmítico no leite bovino, devido a sua posição sn-2 do triacilglicerol, oferece maior estabilidade e baixa massa molecular, portanto, são metabolizados e absorvidos rapidamente (10). É um ácido graxo saturado de 16 carbonos, possui um ponto de fusão de 62,8 °C e um pK de 4,78 (11).
O método tradicionalmente mais utilizado na indústria de alimentos para determinar o teor de gordura no leite é o teste de Gerber, baseado no princípio de destruição das micelas de gordura e a dissolução da caseína, no entanto, é um método perigoso e que necessita de muitas etapas (12,13). Há também equipamentos modernos para análise do teor de gordura, baseados em técnicas cromatográficas e de espectroscopia, entretanto, são métodos dispendiosos que necessitam de equipamentos especializados (14–17).
O termo nanotecnologia é definido como uma tecnologia precisa que utiliza de fenômenos em escala nanométrica, uma área de pesquisa em grande expansão devido a sua capacidade de melhorar a qualidade dos diversos setores industriais no qual essa tecnologia vem sendo inserida, bem como, promover o crescimento econômico (18,19). Introduzidos neste conceito, as nanoestruturas (estruturas com dimensões nanométricas), oferecem diversas aplicações, visto que apresentam propriedades físico-químicas ajustáveis, bem como, uma elevada área superficial que permite aumentar as características de interesse da estrutura (20).
As nanoestruturas metálicas possuem características estruturais únicas e propriedades eletrônicas e físico-químicas importantes, visto que, através da modulação de sua composição, tamanho, forma e estrutura é possível ajustar as propriedades e comportamentos de acordo com a finalidade esperada (21,22). Dentre os vários nanomateriais metálicos, as nanoestruturas de ouro (AuNP) têm atraído um grande interesse para pesquisa devido às suas propriedades ópticas e físicas distintas, uma vez que, de acordo com suas características, principalmente o estado de agregação da molécula, é possível observar a mudança de coloração na nanoestrutura (23).
Dito isso, o objetivo do presente trabalho foi analisar a interação da nanopartícula de ouro com o ácido palmítico, com o intuito de observar a mudança de coloração da solução de acordo com a concentração do ácido graxo, para que futuramente seja possível a criação de um nanossensor colorimétrico para análise do teor de gordura do leite bovino.
MATERIAL E MÉTODOS
Os reagentes utilizados na pesquisa eram de grau de pureza analítico e foram adquiridos em laboratórios do Departamento de Química, Biotecnologia e Engenharia de Bioprocessos – UFSJ/CAP. Todas as soluções aquosas foram preparadas com água destilada. Os espectros de absorção do UV-Vis foram registrados na gama de 700-300 nm no leitor de microplaca Synergy HT (Biotek, EUA).
Síntese de AuNPs
As nanopartículas de ouro foram sintetizadas através da redução de ácido cloroáurico (HAuCl4) mediada por citrato, de acordo com procedimentos previamente publicados (24), com modificações necessárias. Desta forma, 100 mL de uma solução aquosa de HAuCl4 na concentração de 1 mmol L-1 foi preparada e aquecida em um agitador magnético C-MAG HS10 (IKA, Poland) com vigorosa agitação, após a fervura, foi adicionado 10 mL de uma solução de citrato de sódio a 38,8 mmol L-1, momento em que houve a mudança de coloração de amarelo pálido para vermelho escuro. O aquecimento da solução foi mantido por mais 10 minutos e a agitação permaneceu até à temperatura ambiente, posteriormente, a solução foi armazenada a 4 °C. Para a análise, as AuNPs foram diluídas em água destilada na concentração de 1:10 (v/v).
Caracterização das AuNPs
O tamanho hidrodinâmico da nanopartícula, o índice de polidispersão (PDI) e o potencial Zeta foram determinados no Zetasizer PN3702 (Malvern Instruments, UK) via espalhamento de dinâmico de luz. As medidas foram realizadas utilizando um detector de fotodiodo de avalanche e um correlacionador sem qualquer purificação adicional. A fonte de luz foi um laser HeNe de 35 mW e potência de λ = 632,8 nm, linearmente polarizada. Para o controle de intensidade foi empregado um sistema de polarizadores cruzados. O ângulo de detecção foi fixo em 173° e as medidas correlacionadas pelo algoritmo CONTIN.
Preparação do ensaio colorimétrico
Baseado em estudos previamente publicados, foi possível desenvolver e aplicar o método descrito abaixo para a produção da solução de ácido palmítico (25–27). E posteriormente, foi realizado o ensaio colorimétrico, utilizando as nanopartículas de ouro previamente preparadas.
Foi produzida uma amostra de solução padrão e uma amostra de controle, denominada de branco. As concentrações utilizadas no preparo das amostras estão demonstradas na Tabela 1.
Tabela 1 – Concentrações utilizadas para a síntese da solução de ácido palmítico.
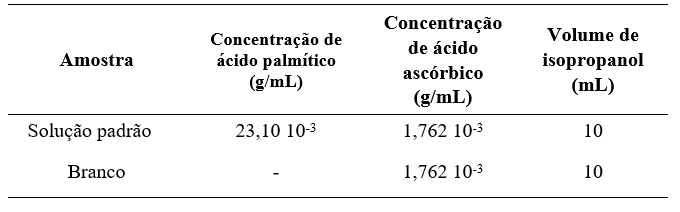
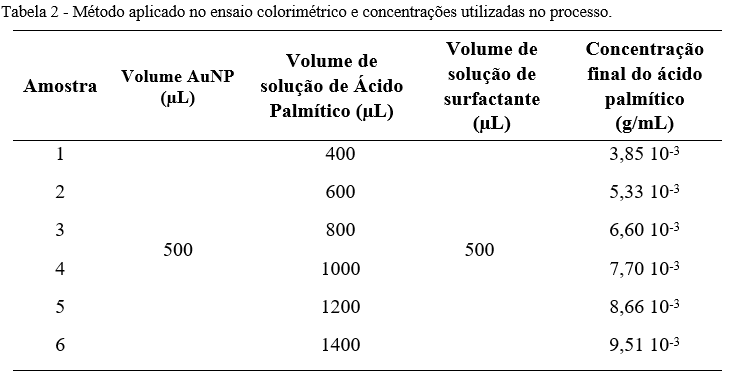
Com a solução de ácido palmítico preparada, foi possível seguir para a próxima etapa, em que se adicionou as nanopartículas de ouro, bem como, uma solução de surfactante (Dodecilbenzeno Sulfonato de Sódio a 10%) para facilitar a solubilização dos compostos. Foram produzidas 6 amostras, com concentrações diferentes, conforme demonstrado na Tabela 3. Para as amostras do controle, utilizou-se 500 µL da solução branco, 500 µL da solução de surfactante e 1500 µL da AuNP.
Fotos das amostras foram tiradas para análise de cores RGB (Red, Green e Blue), utilizando o software PhotoDirector 8, em que 3 pontos de cada amostra foi analisado no histograma, e então, realizou-se a média e o cálculo do valor de cor (CV), posteriormente, as amostras foram filtradas, em filtro de polifluoreto de vinilideno (PVDF) de 0,45 µm para que o filtrado seguisse para a análise de leitura UV-Vis. A medição no espectrofotômetro foi realizada utilizando microplacas de 96 poços, adicionando 200 µL de cada amostra em cada poço da primeira linha da microplaca. Todas as varreduras foram realizadas de 400 a 700 nm, com passo de 1,0 nm por ponto de medição.
RESULTADOS E DISCUSSÃO
As AuNPs sintetizadas apresentaram uma coloração vermelho vivo, um tamanho de 1,2 ± 0,2 nm, PDI de 0,351 ± 0,185 e um potencial zeta de -10,3 ± 3,74 mW. O gráfico de varredura das nanopartículas diluídas 1:10 (v/v) segue representado na Figura 1, onde observa-se um forte pico de absorção em 525 nm, estando de acordo com a literatura (28).
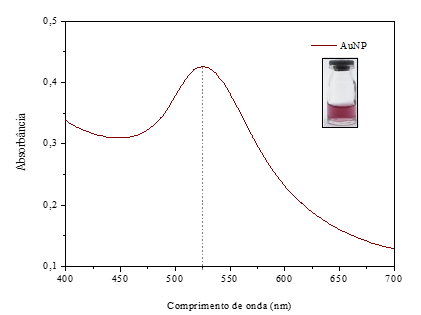
Figura 1 – Perfil espectral de absorção das nanopartículas de ouro obtida no UV-Vis.
Na literatura as nanopartículas metálicas, principalmente as AuNPs, são exploradas para determinação colorimétrica óptica de diferentes tipos de substâncias, baseado na mudança de coloração destas nanopartículas quando em contato com um analito específico (29–35). No entanto, até o presente momento, não foi relatado a utilização de nanopartículas de ouro para detecção colorimétrica de ácidos graxos. Portanto, as AuNPs foram utilizadas para detecção colorimétrica do ácido palmítico (C:16), seguindo a metodologia citada acima. Os resultados visuais estão demonstrados na Figura 2, onde observa-se que com o aumento das concentrações de ácido palmítico, ocorreu uma mudança na coloração do vermelho para o azul, sendo comprovado nas análises de imagem RGB e no espectrofotômetro UV-Vis.

A mudança de coloração foi quantificada a partir do histograma obtido no software PhotoDirector 8, em que foi analisado as diferentes combinações das cores vermelho, verde e azul e a reprodução de um largo espectro cromático. Para isso, utilizou-se da Equação 1, onde avaliou a intensidade do componente vermelho comparado com à intensidade total dos componentes vermelho, verde e azul (36). A escala padrão RGB é determinada por números inteiros, de 0 a 225, para cada uma das três cores, sendo que o número (0,0,0) representa a coloração preta e (255,255,255) corresponde à cor branca (37).
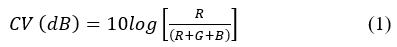
Em que, R, G e B representam a intensidade óptica do vermelho, verde e azul, respectivamente.
Na Tabela 3, estão representados os valores médios de RGB, bem como os valores de CV de cada amostra. Os parâmetros de CV estão representados na Figura 3 em função das concentrações de ácido palmítico.
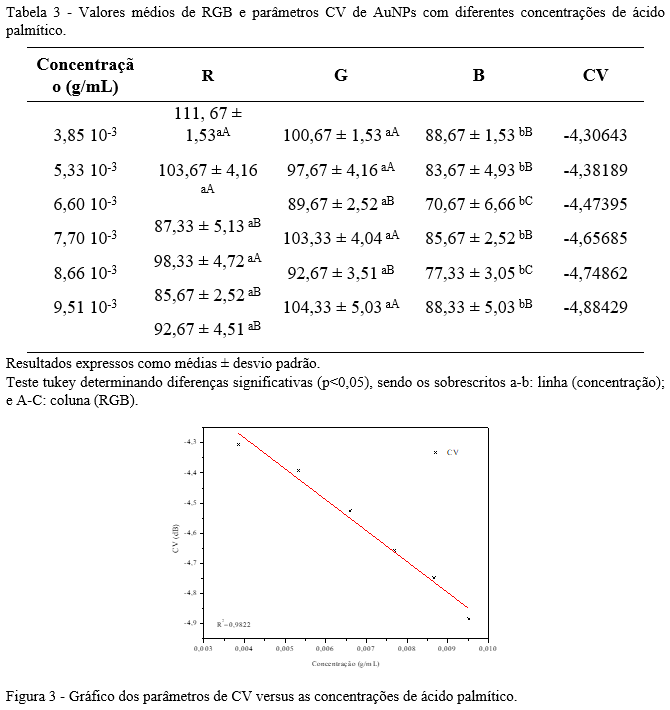
Foi estabelecida uma excelente correlação linear (R2 = 0,9822) entre as diferentes concentrações de ácido palmítico e os parâmetros CV, portanto, observa-se que à medida que a concentração de ácido palmítico aumenta, os parâmetros CV diminuem, demonstrando que mais componentes vermelhos estão sendo absorvidos a partir da agregação dos componentes da amostra.
Os elétrons livres das nanopartículas de ouro estão confinados em seu espaço de acordo com seu tamanho, e consequentemente, possui uma frequência de oscilação, quando um feixe de ondas eletromagnéticas irradia sobre a nanopartícula, o campo elétrico oscilante faz com que os elétrons de condução oscilem em conjunto, processo esse denominado de ressonância de plasmon de superfície localizada (RPSL) (38,39). A RPSL é capaz de gerar a interação ressonante dos elétrons livres da nanoestrutura com o campo eletromagnético oscilante da luz em comprimentos de onda visível (40). Portanto, para complementar a análise dos resultados, a técnica de espectroscopia na região visível foi utilizada na verificação dos processos que envolve os elétrons no efeito de RPSL, bem como a interação da nanoestrutura de ouro com o ácido palmítico. Os resultados estão representados na Figura 4, onde observa-se que à medida que a concentração do ácido palmítico aumenta, o forte pico de absorbância formado em 525 nm diminui, de forma que, nas concentrações máximas (f e g) não há formação de um pico, demonstrando assim que houve alteração na coloração das amostras.
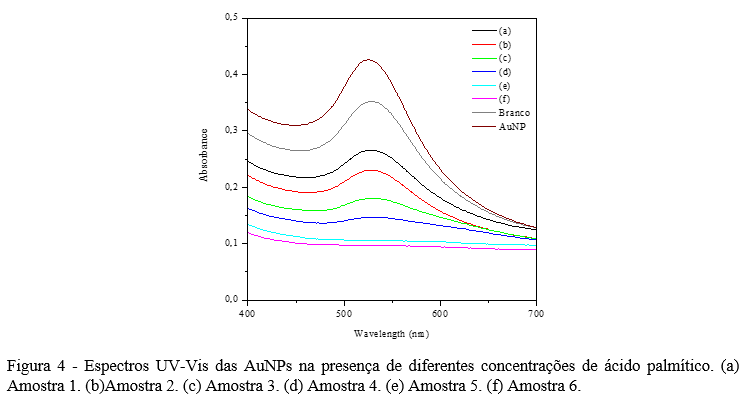
A interação de lipídios com AuNps foi relatada em um estudo utilizando nanopartículas de ouro com tamanho de 1,284 nm, correspondente com o tamanho da nanoestrutura utilizado no presente trabalho, em que a penetração das AuNPs na camada lipídica induz a mudança estrutural no nanocomposto (41). Há uma correlação forte entre o pico de ressonância de plasmon de superfície localizada e a estrutura da nanopartícula (42). O ácido ascórbico trata-se de um agente redutor, estudos apontaram a capacidade desta substância de reduzir as nanopartículas de ouro, bem como auxiliar na estabilidade da molécula (43–45). Portanto, o ácido palmítico, quando em contato com as AuNPs, pode ter induzido a mudança estrutural na nanopartícula, com o auxílio do ácido ascórbico, e consequentemente, afetado a coloração da amostra, como observados nos métodos quantitativos de RGB e espectroscopia.
CONCLUSÕES
Conclui-se com o presente trabalho que as nanopartículas de ouro possuem um grande potencial para detecção colorimétrica de ácidos graxos, os resultados apresentados de RBG foi complementado com a espectroscopia UV-Vis, onde foi possível verificar a mudança de coloração das amostras. Para aplicação na indústria de laticínios, estudos utilizando diferentes ácidos graxos devem ser realizados, bem como, a análise em amostra real. No entanto, este estudo se mostrou promissor para a produção de um nanosensor colorimétrico para detecção de gordura no leite bovino.
AGRADECIMENTOS
Agradeço à Universidade Federal de São João del-Rei por fornecer laboratórios e reagentes para a realização deste trabalho. À FAPEMIG, CNPq e CAPES por todo apoio financeiro prestado.
REFERÊNCIAS
- Alothman M, Hogan SA, Hennessy D, Dillon P, Kilcawley KN, O’Donovan M, et al. The “Grass-Fed” Milk Story: Understanding the Impact of Pasture Feeding on the Composition and Quality of Bovine Milk. Foods 2019, Vol 8, Page 350 [Internet]. 2019 Aug 17 [cited 2023 Mar 26];8(8):350. Available from: https://www.mdpi.com/2304-8158/8/8/350/htm
- Foroutan A, Guo AC, Vazquez-Fresno R, Lipfert M, Zhang L, Zheng J, et al. Chemical Composition of Commercial Cow’s Milk. J Agric Food Chem [Internet]. 2019 May 1 [cited 2023 Mar 26];67(17):4897–914. Available from: https://pubs.acs.org/doi/full/10.1021/acs.jafc.9b00204
- Beber CL, Langer G, Meyer J. Strategic Actions for a Sustainable Internationalization of Agri-Food Supply Chains: The Case of the Dairy Industries from Brazil and Germany. Sustainability 2021, Vol 13, Page 10873 [Internet]. 2021 Sep 30 [cited 2023 Mar 27];13(19):10873. Available from: https://www.mdpi.com/2071-1050/13/19/10873/htm
- MAPA. Mapa do Leite — Ministério da Agricultura e Pecuária [Internet]. 2022 [cited 2023 Mar 27]. Available from: https://www.gov.br/agricultura/pt-br/assuntos/producao-animal/mapa-do-leite
- Priyashantha H, Lundh Å. Graduate Student Literature Review: Current understanding of the influence of on-farm factors on bovine raw milk and its suitability for cheesemaking. J Dairy Sci. 2021 Nov 1;104(11):12173–83.
- Hageman JHJ, Danielsen M, Nieuwenhuizen AG, Feitsma AL, Dalsgaard TK. Comparison of bovine milk fat and vegetable fat for infant formula: Implications for infant health. Int Dairy J. 2019 May 1;92:37–49.
- Kailasapathy K. Chemical Composition, Physical, and Functional Properties of Milk and Milk Ingredients. Dairy Processing and Quality Assurance [Internet]. 2015 Oct 30 [cited 2023 Apr 27];77–105. Available from: https://onlinelibrary.wiley.com/doi/full/10.1002/9781118810279.ch04
- Djordjevic J, Ledina T, Baltic MZ, Trbovic D, Babic M, Bulajic S. Fatty acid profile of milk. IOP Conf Ser Earth Environ Sci [Internet]. 2019 Sep 1 [cited 2023 Apr 30];333(1):012057. Available from: https://iopscience.iop.org/article/10.1088/1755-1315/333/1/012057
- Tiplady KM, Lopdell TJ, Sherlock RG, Johnson TJJ, Spelman RJ, Harris BL, et al. Comparison of the genetic characteristics of directly measured and Fourier-transform mid-infrared-predicted bovine milk fatty acids and proteins. J Dairy Sci. 2022 Dec 1;105(12):9763–91.
- Viriato RLS, Queirós M de S, Macedo GA, Ribeiro APB, Gigante ML. Design of new lipids from bovine milk fat for baby nutrition. https://doi.org/101080/1040839820201813073 [Internet]. 2020 [cited 2023 May 1];62(1):145–59. Available from: https://www.tandfonline.com/doi/abs/10.1080/10408398.2020.1813073
- Innis SM. Palmitic Acid in Early Human Development. https://doi.org/101080/1040839820151018045 [Internet]. 2016 Sep 9 [cited 2023 May 1];56(12):1952–9. Available from: https://www.tandfonline.com/doi/abs/10.1080/10408398.2015.1018045
- Stefanov I, Vlaeminck B, Fievez V. A novel procedure for routine milk fat extraction based on dichloromethane. Journal of Food Composition and Analysis. 2010 Dec 1;23(8):852–5.
- Desai P, Pandya U. Review on Reference & Routine Measurement Techniques of Milk Fat based on Process, Cost and Instrumentation. 2022 [cited 2023 May 2]; Available from: https://www.researchgate.net/profile/Pankti-Desai-6/publication/364405526_Review_on_Reference_Routine_Measurement_Techniques_of_Milk_Fat_based_on_Process_Cost_and_Instrumentation/links/6351562296e83c26eb3ad95c/Review-on-Reference-Routine-Measurement-Techniques-of-Milk-Fat-based-on-Process-Cost-and-Instrumentation.pdf
- Mendoza LG, González-Álvarez J, Gonzalo CF, Arias-Abrodo P, Altava B, Luis S V., et al. Gas chromatographic analysis of fatty acid methyl esters of milk fat by an ionic liquid derived from L-phenylalanine as the stationary phase. Talanta. 2015 Oct 1;143:212–8.
- Gastaldi D, Medana C, Giancotti V, Aigotti R, Dal Bello F, Baiocchi C. HPLC-APCI analysis of triacylglycerols in milk fat from different sources. European Journal of Lipid Science and Technology [Internet]. 2011 Feb 1 [cited 2023 May 3];113(2):197–207. Available from: https://onlinelibrary.wiley.com/doi/full/10.1002/ejlt.201000068
- Bogomolov A, Melenteva A. Scatter-based quantitative spectroscopic analysis of milk fat and total protein in the region 400–1100 nm in the presence of fat globule size variability. Chemometrics and Intelligent Laboratory Systems. 2013 Jul 15;126:129–39.
- Haque F, Bubli SY, Khan MS. UV–Vis Spectroscopy for Food Analysis. 2021 [cited 2023 May 3];169–93. Available from: https://link.springer.com/chapter/10.1007/978-3-030-68636-9_8
- Haleem A, Javaid M, Singh RP, Rab S, Suman R. Applications of nanotechnology in medical field: a brief review. Global Health Journal. 2023 Feb 25;
- Kumar R, Kumar M, Luthra G. Fundamental approaches and applications of nanotechnology: A mini review. Mater Today Proc. 2023 Jan 2;
- Nasrollahzadeh M, Issaabadi Z, Sajjadi M, Sajadi SM, Atarod M. Types of Nanostructures. Interface Science and Technology. 2019 Jan 1;28:29–80.
- Zhao Z, To S, Wang J, Zhang G, Weng Z. A review of micro/nanostructure effects on the machining of metallic materials. Mater Des. 2022 Dec 1;224:111315.
- Ou X, Liu Y, Zhang M, Hua L, Zhan S. Plasmonic gold nanostructures for biosensing and bioimaging. Microchimica Acta 2021 188:9 [Internet]. 2021 Aug 25 [cited 2023 May 11];188(9):1–15. Available from: https://link.springer.com/article/10.1007/s00604-021-04964-1
- Anh NH, Doan MQ, Dinh NX, Huy TQ, Tri DQ, Ngoc Loan LT, et al. Gold nanoparticle-based optical nanosensors for food and health safety monitoring: recent advances and future perspectives. RSC Adv [Internet]. 2022 Apr 7 [cited 2023 May 9];12(18):10950–88. Available from: https://pubs.rsc.org/en/content/articlehtml/2022/ra/d1ra08311b
- Grabar KC, Hommer MB, Natan MJ, Freeman RG. Preparation and Characterization of Au Colloid Monolayers. Anal Chem [Internet]. 1995 [cited 2023 Mar 28];67(4):735–43. Available from: https://pubs.acs.org/doi/abs/10.1021/ac00100a008
- Calvo B, Collado I, Cepeda EA. Solubilities of palmitic acid in pure solvents and its mixtures. J Chem Eng Data [Internet]. 2009 Jan 8 [cited 2023 May 22];54(1):64–8. Available from: https://pubs.acs.org/doi/full/10.1021/je8005979
- Torres P, Kunamneni A, Ballesteros A, Plou FJ. Enzymatic Modification for Ascorbic Acid and Alpha-Tocopherol to Enhance their Stability in Food and Nutritional Application. The Open Food Science Journal. 2008 Mar 25;2(1):1–9.
- Moribe K, Limwikrant W, Higashi K, Yamamoto K. Drug Nanoparticle Formulation Using Ascorbic Acid Derivatives. J Drug Deliv. 2011;2011.
- Creighton JA, Eadon DG. Ultraviolet-visible absorption spectra of the colloidal metallic elements. Journal of the Chemical Society, Faraday Transactions. 1991;87(24):3881–91.
- Kumar N, Seth R, Kumar H. Colorimetric detection of melamine in milk by citrate-stabilized gold nanoparticles. Anal Biochem. 2014 Jul 1;456(1):43–9.
- Zhou D, Xie G, Cao X, Chen X, Zhang X, Chen H. Colorimetric determination of staphylococcal enterotoxin B via DNAzyme-guided growth of gold nanoparticles. Microchimica Acta [Internet]. 2016 Oct 1 [cited 2023 May 14];183(10):2753–60. Available from: https://link.springer.com/article/10.1007/s00604-016-1919-z
- Li X, Cheng R, Shi H, Tang B, Xiao H, Zhao G. A simple highly sensitive and selective aptamer-based colorimetric sensor for environmental toxins microcystin-LR in water samples. J Hazard Mater [Internet]. 2016 Mar 5 [cited 2023 May 14];304:474–80. Available from: https://pubmed.ncbi.nlm.nih.gov/26619046/
- Amini B, Kamali M, Salouti M, Yaghmaei P. Spectrophotometric, colorimetric and visually detection of Pseudomonas aeruginosa ETA gene based gold nanoparticles DNA probe and endonuclease enzyme. Spectrochim Acta A Mol Biomol Spectrosc. 2018 Jun 15;199:421–9.
- Ma Q, Wang Y, Jia J, Xiang Y. Colorimetric aptasensors for determination of tobramycin in milk and chicken eggs based on DNA and gold nanoparticles. Food Chem. 2018 May 30;249:98–103.
- Zhang Y, Lu T, Wang Y, Diao C, Zhou Y, Zhao L, et al. Selection of a DNA Aptamer against Zearalenone and Docking Analysis for Highly Sensitive Rapid Visual Detection with Label-Free Aptasensor. J Agric Food Chem. 2018 Nov 14;66(45):12102–10.
- madkour E, Abou Zeid A, Abdel Ghany S, Alshehrei FM, EL- Ghareeb D, Abdel-Hakeem M. Sensitive and selective colorimetric detection of Staphylococcus aureus-SPA gene by engineered gold nanosensor. Saudi J Biol Sci. 2023 Feb 1;30(2):103559.
- Zheng B, Li J, Zheng Z, Zhang C, Huang C, Hong J, et al. Rapid colorimetric detection of arsenic (III) by glutathione functionalized gold nanoparticles based on RGB extracting system. Opt Laser Technol. 2021 Jan 1;133:106522.
- Rajamanikandan R, Ilanchelian M. Simple smartphone merged rapid colorimetric platform for the environmental monitoring of toxic sulfide ions by cysteine functionalized silver nanoparticles. Microchemical Journal. 2022 Mar 1;174:107071.
- Akshaya K, Arthi C, Pavithra AJ, Poovizhi P, Antinate SS, Hikku GS, et al. Bioconjugated gold nanoparticles as an efficient colorimetric sensor for cancer diagnostics. Photodiagnosis Photodyn Ther. 2020 Jun 1;30.
- Ai K, Huang J, Xiao Z, Yang Y, Bai Y, Peng J. Localized surface plasmon resonance properties and biomedical applications of copper selenide nanomaterials. Mater Today Chem. 2021 Jun 1;20.
- Xu W, Liu H, Zhou D, Chen X, Ding N, Song H, et al. Localized surface plasmon resonances in self-doped copper chalcogenide binary nanocrystals and their emerging applications. Nano Today. 2020 Aug 1;33:100892.
- Lin X, Li Y, Gu N. Nanoparticle’s size effect on its translocation across a lipid bilayer: A molecular dynamics simulation. J Comput Theor Nanosci [Internet]. 2010 Jan [cited 2023 May 26];7(1):269–76. Available from: https://www.researchgate.net/publication/52005286_Nanoparticle’s_Size_Effect_on_Its_Translocation_Across_a_Lipid_Bilayer_A_Molecular_Dynamics_Simulation
- Li CH, Chan MH, Chang YC, Hsiao M. Gold Nanoparticles as a Biosensor for Cancer Biomarker Determination. Molecules 2023, Vol 28, Page 364 [Internet]. 2023 Jan 2 [cited 2023 May 27];28(1):364. Available from: https://www.mdpi.com/1420-3049/28/1/364/htm
- Sun X, Yang Y, Zhang Z, Qin D. Mechanistic Roles of Hydroxide in Controlling the Deposition of Gold on Colloidal Silver Nanocrystals. Chemistry of Materials. 2017 May 9;29(9):4014–21.
- Selva Sharma A, SasiKumar T, Ilanchelian M. A Rapid and Sensitive Colorimetric Sensor for Detection of Silver Ions Based on the Non-aggregation of Gold Nanoparticles in the Presence of Ascorbic Acid. J Clust Sci [Internet]. 2018 Jul 1 [cited 2023 May 27];29(4):655–62. Available from: https://link.springer.com/article/10.1007/s10876-018-1375-5
- Nikoobakht B, El-Sayed MA. Preparation and growth mechanism of gold nanorods (NRs) using seed-mediated growth method. Chemistry of Materials. 2003 May 20;15(10):1957–62.