
EXTRAÇÃO DE COMPOSTOS FENÓLICOS POR FLUIDO SUPERCRÍTICO: REVISÃO DE LITERATURA
Capítulo de livro publicado no livro do VIII ENAG E CITAG. Para acessa-lo clique aqui.
DOI: https://doi.org/10.53934/9786585062046-36
Este trabalho foi escrito por:
Ivânia Samara dos Santos Silva *; Amélia Ruth Nascimento Lima ;Maria Tereza Lucena Pereira ; Maria Carla Candido da Silva ; Lucas Monteiro Bezerra Pinheiro ; Haíssa Roberta Cardarelli ; Carolina Lima Cavalcanti de Albuquerque
*[email protected] Autor correspondente (Corresponding author) – Email:
Resumo: Dentre os fitoquímicos com atividades bioativas se destacam os compostos fenólicos, que exercem diversas funcionalidades tanto em âmbito tecnológico, como também biológico. Apesar de serem abundantes nos vegetais sua extração apresenta alguns desafios, os métodos de extração convencionais não conseguem realizar esse processo de forma satisfatória, desta forma, a extração por fluido supercrítico se mostra uma alternativa promissora, pois é considerada uma tecnologia verde, além de suas características de versatilidade, seletividade e tempo de extração relativamente curto. No entanto, para que a extração de fenólicos seja eficiente, deve-se analisar os parâmetros de equilíbrio, e cinética de extração, que estão correlacionados com as condições experimentais empregadas de temperatura, pressão, vazão e uso de cossolvente ou não, já que são moléculas polares e o solvente utilizado apresenta baixa solubilidade a substâncias polares. Desta forma, o objetivo dessa revisão é apontar os principais parâmetros utilizados na extração de compostos fenólicos por meio da tecnologia de fluido supercrítico (SFE) a fim de nortear as futuras pesquisas de aplicação.
Palavras–chave: compostos bioativos; condições supercríticas; dióxido de carbono
Abstract: Among the phytochemicals with bioactive activities, phenolic compounds stand out, they exert several functionalities both technological and biological. Although they are abundant in vegetables, their extraction presents some challenges; the conventional extraction methods are not able to perform this process satisfactorily, thus, the supercritical fluid extraction is a promising alternative, because it is considered a green technology, besides its versatility, selectivity and relatively short extraction time characteristics. However, for the extraction of phenolics to be efficient, it is necessary to analyze the equilibrium parameters and extraction kinetics, which are correlated with the experimental conditions of temperature, pressure, flow rate and the use of a solvent or not, since they are polar molecules and the solvent used presents low solubility to polar substances. Thus, the objective of this review is to point out the main parameters used in the extraction of phenolic compounds by means of supercritical fluid technology (SFE) in order to guide future research applications.
Keywords: bioactive compouds; supercritical conditions; carbon dioxide
INTRODUÇÃO
A indústria de alimentos tem sido cada vez mais cotada para o desenvolvimento de produtos com virtudes funcionais em decorrência da crescente exigência dos consumidores por alimentos que sejam capazes de ofertar além de nutrientes, compostos ativos, que são substâncias promotoras de benefícios a saúde (1-2).
Dentre os componentes bioativos que se destacam, estão os compostos fenólicos, que representam um dos mais abundantes grupos fitoquímicos nos vegetais, tendo grande importância fisiológica e morfológica nas plantas (3) além dessas funções, eles também apresentam diversas atividades, como, potenciais indícios de efeitos prebióticos e aumento da viabilidade de microrganismos (4) atividades biológicas, efeito antioxidante, antitumoral e consequente diminuição dos riscos de doenças crônicas e degenerativas, apresentam também, atividades tecnológicas, como, ação antimicrobiana, melhora de vida de prateleira e fornecimento de características específicas como textura, cor e sabor aos produtos (5-6).
Várias partes das plantas, frutas e seus resíduos (casca, caroços e bagaço) que podem ser provenientes do processamento industrial vêm sendo estudadas, tanto na aplicação direta, como também na produção de extratos ou óleos produzidos, visando os compostos fenólicos (7-8).
Existem diversos métodos de extração desses fitoquímicos; os métodos mais comuns são, maceração, prensagem, Soxhlet, destilação (9-11). No entanto, a maioria desses processos envolvem aquecimento elevado, que podem gerar degradação térmica dos compostos de interesse, além do que, necessitam de altas demandas de tempo, energia ou quantidades de solventes elevados (12). Desta forma, vários métodos de extração foram atualizados, com o intuito de melhorar o tempo, custo, rendimento, reduzir impacto ambiental e menor perda de bioativos (13), dentre eles, pode-se citar a extração por fluido supercrítico (SFE– Supercritical Fluid Extraction).
A SFE é reconhecida como uma tecnologia avançada, sendo capaz de extrair compostos de interesse com alta eficiência graças a sua seletividade, pode gerar baixo custo operacional e bom rendimento, além disso, é considerada uma tecnologia verde, pois é livre de solventes tóxicos, demostrando indicativo de baixa toxicidade (14). A capacidade das condições supercríticas de densidade semelhante a líquidos, a alta difusividade e viscosidade semelhante a gás, fazem com que seu poder de solvatação consiga permear de forma mais eficaz a amostra (15).
O dióxido de carbono (CO2) é o gás mais utilizado no SFE devido sua facilidade para atingir o ponto crítico, sensibilidade, pureza e custo (16). No entanto, a solubilidade de substâncias polares em CO2 é baixa, mas que pode ser contornada com uma pequena quantidade de cossolvente de média ou alta polaridade adicionado ao CO2, como etanol ou água, que são geralmente reconhecidos como seguros (GRAS) (17-19). A escolha adequada do solvente, das condições de temperatura e pressão são um dos parâmetros mais influentes para o sucesso do processo de extração dos compostos de interesse (20).
O objetivo dessa revisão foi apontar os principais parâmetros utilizados na extração de compostos fenólicos por meio da tecnologia de fluido supercrítico (SFE). Essa revisão ajudará a preencher as lacunas existem da tecnologia SFE voltadas para os compostos fenólicos, tendo em vista que a maioria dos estudos consolidados focam apenas na extração de lipídeos. Além do que, esse estudo também poderá ser usado para direcionar pesquisas futuras, refinando então os parâmetros a serem utilizados.
COMPOSTOS FENÓLICOS
Os compostos fenólicos ou polifenóis são metabólicos secundários encontrados nos tecidos vegetais, desde as raízes, flores, sementes, folhas e partes comestíveis (3). São componentes que estão relacionados com o sistema de defesa das plantas (proteção contra raios ultravioletas, patógenos e alguns predadores), apresentam também função estrutural e adaptação ao ambiente. Além disso, os compostos fenólicos colaboram para as características sensoriais das frutas e vegetais (21).
São reconhecidos como moléculas com um ou mais anéis aromáticos, que podem ser acoplados a um grupo hidroxila (monohidroxilados) ou mais (poli-hidroxilados) (22). Já foram caracterizadas cerca de 8.000 moléculas, apresentando uma grande diversidade na estrutura, as estruturas encontradas variam entre 200 a 3.500 kDa (23).
De acordo com o número de arranjo de átomos eles são categorizados e divididos em dois grandes grupos, os flavonóides e os não flavonóides (ácidos fenólicos) (3). Diante das particularidades estruturais esses grupos são subdivididos em diferentes classes, que vão desde fenólicos mais simples, como os ácidos fenólicos a estruturas maiores como os taninos (24).
Além de apresentar extrema importância para as plantas, esses fitoquímicos demonstram efeitos bioativos, sendo amplamente visados e estudados por seus benefícios terapêuticos e ou profiláticos (25).
Uma das suas funções mais estabelecidas é a de exercer efeito antioxidante; esses compostos conseguem sequestrar espécies reativas de oxigênio e nitrogênio, apresentam ação na quelação de metais pro-oxidantes e atuam na regeneração de outros antioxidantes, o que leva a efeitos contra danos oxidativos, como problemas cardiovasculares e doenças degenerativas (26). Outras propriedades também já foram encontradas, como, ação antiinflamatória e diminuição da incidência de obesidade, efeito antitumoral, correlação com a diminuição da ocorrência de diabetes (27), efeito de modulação intestinal, apresentando potencial prebiótico (28).
Além disso, na indústria de alimentos os compostos fenólicos também apresentam diversas aplicações tecnológicas, usados como aditivos naturais pela ação antioxidante na estabilização da rancidez dos produtos, ação contra danos nitrooxidativos nos produtos e consequente aumento de vida de prateleira (5). Também já foi demostrado ação no aumento da viabilidade de microorganismos probióticos durante o armazenamento, além de mudanças positivas nas características sensoriais dos produtos (29).
No entanto, apesar de serem abundantes nos vegetais a utilização é dificultada pela grande heterogeneidade na natureza química das frações fenólicas, presença de compostos interferentes, tamanho das partículas e condições de armazenamento. Logo, a extração se torna uma etapa crítica (30).
Existem diversos métodos de extração desses fitoquímicos, que se baseiam basicamente em operações entre a transferência de massas em uma dada matriz com a finalidade de separar o composto de interesse. Essas operações podem ocorrer através de processos mecânicos, físicos ou químicos, que podem variar desde a parte da planta a ser utilizado, como também, a finalidade do produto (9), sendo um passo muito importante para a recuperação e a purificação desses compostos (13).
Esses componentes geralmente são extraídos por processos convencionais, como por exemplo Soxhlet, maceração, prensagem e hidrodestilação, utilizando solventes orgânicos (10-11,13,31). Porém, os solventes orgânicos são frequentemente tóxicos, podendo ficar resquícios nos produtos, demandam altas temperaturas podendo degradar as moléculas termolábeis, e alto consumo de tempo e energia durante o processo (32).
Para superar esses entraves, novas formas de extração vêm sendo empregadas, e entre as mais notáveis está a extração com fluido supercrítico (33).
EXTRAÇÃO POR FLUIDO SUPERCRITICO
As primeiras aplicações de Supercritical Fluid Extraction (SFE) ocorreram na indústria de alimentos na década de 1970 (34), conforme as evoluções tecnológicas, o método foi se refinando e possibilitando o isolamento de certos compostos de interesse, coletando as frações desejadas e removendo os compostos não desejados de um componente (35).
Em termos gerais, entende-se a SFE como um mecanismo unitário que permite a separação de um soluto dentro de uma mistura complexa de compostos pertencentes a uma matriz biológica sólida, por meio de um solvente adequado (36).
Pelas características versáteis, seletividade, tempo relativamente curto de extração e vantagens ambientais (tecnologia verde), o SFE é um método de extração promissor (37).
Existem vários solventes que podem ser usados e a escolha dependerá dos compostos biológicos ao qual se almeja. Dentre eles, o dióxido de carbono supercrítico (sc-CO2) é o mais comumente utilizado, que se sobressai por apresentar constantes críticas baixas (Tc (temperatura crítica) = 31,1 ° C; Pc (pressão crítica) = 7,38 MPa (Mega Pascal)), não apresenta toxidade, não é inflamável, não mutagênico, demonstra características termoestáveis e apresenta custo acessível. Além disso, esse gás apresenta alto coeficiente de difusão e vaporização, onde os produtos obtidos via sc-CO2 apresentam-se livres do solvente de extração (32,38).
Devido ao seu caráter apolar, o sc-CO2 geralmente é usado para extrair compostos hidrofóbicos, como óleos essenciais, tocoferóis, e compostos levemente hidrofílicos, como alguns compostos fenólicos de baixo peso molecular. Para se extrair compostos de caráter hidrofílicos, utilizam-se mudanças na pressão do procedimento, ou pode-se alterar a polaridade de solventes com o uso de cossolventes, como etanol e água (14).
Para que a extração seja eficiente na matriz vegetal, deve-se analisar os parâmetros de equilíbrio e cinética de extração, que estão correlacionados com as condições experimentais empregadas. Os principais aspectos que interferem no processo e na qualidade de extração são a pressão, a temperatura, a vazão do solvente, o tipo e quantidade do cossolvente utilizado (36).
O conhecimento sobre os aspectos químicos de extração dos compostos bioativos pode permitir a seleção e uma melhor aplicação das moléculas bioativas; os extratos obtidos via essa técnica são considerados Generally Recognized As Safe (GRAS) pela American Food and Drug Administration, ou seja, pode ser aplicado a diversos alimentos sem acarretar efeitos indesejáveis à saúde, o que entra em concordância com a necessidade atual da indústria farmacêutica e alimentícia (32).
PRINCIPAIS PARÂMETROS UTILIZADOS PARA A EXTRAÇÃO DE FENÓLICOS POR SFE
Foram selecionados 13 artigos nas bases de dados Google Acadêmico, Science Direct e Scopus que usaram o SFE-CO2 com objetivo de extrair os compostos fenólicos, examinando a interferência dos principais parâmetros de extração e sua correlação com esses bioativos. Em todos os artigos selecionados foram analisados os compostos fenólicos totais e atividade antioxidante.
Pela grande diversidade de natureza química das moléculas fenólicas, os parâmetros podem variar muito entre um vegetal e outro e até mesmo entre as partes dos vegetais e objetivos de aplicação.
Em relação a pressão utilizada nos estudos, obteve-se um intervalo entre 10 a 35 MPa, na maioria das pesquisas foi feito a comparação entre duas ou mais pressões, como pode ser observado no Quadro 1.
A densidade do fluido supercrítico e consequente poder de solvatação aumenta quando se eleva a pressão, no entanto, também pode levar a diminuição da seletividade da extração (36). Logo, a faixa de pressão dependerá muito do material biológico e composto alvo.
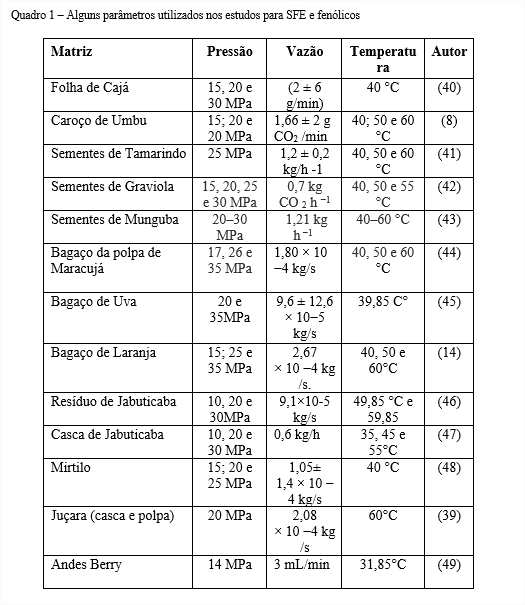
Em relação a vazão (quantidade de solvente que passa por todo o sistema durante o tempo de extração) também variou bastante (Tabela 1); de maneira geral, a vazão é estabelecida por testes pilotos nos estudos, relacionados ao tempo de extração e rendimento global. O uso de vazões mais elevadas pode interferir no rendimento geral devido ao pouco tempo de contato necessário para atingir a saturação do solvente. No entanto, baixas pressões podem afetar a extração dos solutos, já que pode interferir no coeficiente de dispersão e transferência de massa (50).
A temperatura é um dos fatores mais importantes, interfere diretamente no poder da migração de massa e quanto mais alto a temperatura, maior a pressão de vapor do soluto, o que consequentemente, pode aumentar a solubilidade, em contra partida, a densidade do solvente diminui, fazendo com que a capacidade de solvatação seja mais baixa (14). Desta maneira, a temperatura precisa ser ponderada para atingir uma boa extração.
Como pode-se observar no Quadro 1, a temperatura ficou na faixa de 31,85 a 60 °C, a temperatura mais baixa (31,85 °C) encontrada é próxima da temperatura mínima para que o CO2 atinja o ponto supercrítico, e a temperatura mais elevada (60 °C) geralmente é vista como temperatura limite, já que os compostos fenólicos são termolábeis (36).
USO DE COSSOLVENTES NA SFE
O uso de cossolventes ou modificadores é recorrido na SFE para fenólicos, devido ao CO2 apresentar baixa afinidade por compostos polares. Porém, o grau de modificação da polaridade é relacionado com o tipo de cossolvente utilizado na extração SFE (36). De forma geral, podem ser utilizados diversos tipos de cossolvente, como por exemplo, metanol, mas, para fins de consumo humano, na indústria farmacêutica e de alimentos isso poderia inviabilizar o uso, além do que, iria contra a teoria GRAS; logo os cossolventes mais usados são os que não acarretam risco de toxicidade caso fique resquícios desses componentes após o processo.
Na Figura 1, pode ser visto os cossolventes mais empregados nas análises de SFE para compostos fenólicos.
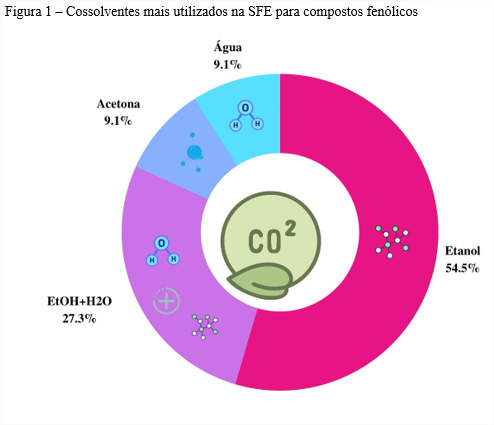
Foi observado que o cossolvente mais comumente empregado foi o etanol (54,5%), seguidos da combinação entre etanol e água (27,3%). Isso provavelmente se deu porque o etanol geralmente apresenta bons rendimentos em extração a baixa pressão, que muitas vezes serve como parâmetro para os diversos estudos. Além do que, o etanol tem baixa toxicidade e é de fácil evaporação (40).
MELHORES RESULTADOS DAS CONDIÇÕES EMPREGADAS NA SFE E FENÓLICOS
Além da alta heterogeneidade dos fenólicos, existe uma alta correlação entre as diversas condições e combinações a serem empregadas na SFE e sua variável resposta. Desta maneira, na Figura 2, podem ser observadas as combinações desses fatores que obtiveram os melhores resultados em relação aos fenólicos totais e atividade antioxidante.

Como pode ser observado (Figura 2) quando usado sementes como matéria prima para a extração, o uso de cossolvente foi dispensado (8, 41-43), talvez por apresentarem menos substâncias apolares e a introdução de modificadores não seja relevante.
Em relação ao uso de cossolventes, todos os artigos que analisaram a eficiência entre o etanol puro e combinações entre etanol e água (EtOH+H2O) demostraram melhor eficiência entre o uso combinado (14,40,48).
A água apresenta maior polaridade do que o etanol, dessa forma, combinações entre esses dois cossolventes tem maior polaridade do que o etanol isolado e menor do que a água isolada. No entanto, a água utilizada em maiores quantidade pode gelificar a matéria prima que possuir fibras solúveis na sua composição por essas razões o uso combinado pode aumentar a extração dos biocompostos polares e de maior atividade antioxidante sem comprometer a matéria-prima (14).
Vazões acima de 30 MPa (14, 44-45) mostraram não serem relevantes para a resposta do processo, sobressaindo-se então faixas de até 30 MPa como melhores resultados para o processo de extração em questão. As matérias-primas ricas em antocianinas (pigmentos de cor vermelho vivo ao violeta/azul) demostraram que pressões mais brandas (14- 20 MPa) conseguem exibir bons resultados.
CONCLUSÕES
Foi possível observar que na SFE para fenólicos existem algumas dificuldades a serem enfrentadas. O fato de os compostos apresentarem sensibilidade a temperatura pode limitar a extração, não sendo então, recomendado temperaturas acima de 60 °C. Em relação à pressão, vazões acima de 30 MPa não apresentaram relevância nos resultados das extrações.
Por serem compostos polares, o uso de cossolventes é necessário na maioria dos casos, no entanto, foi apontado que o uso de cossolvente talvez possa ser dispensado quando for usado sementes como matéria-prima. Outro fator importante a ser destacado, é que o uso de cossolvente combinados (água e etanol) apresentaram melhores resultados quando comparado ao cossolvente puro.
Diante da grande diversidade das fontes e do tipo de compostos fenólicos alvo, fica evidente que para que o processo de extração seja eficiente é importante planejar, estudar e testar os parâmetros a serem utilizados, pois os fatores temperatura, pressão, vazão, uso de cossolvente ou não, podem ser interdependentes, razão pela qual é imprescindível analisar cada caso particular.
REFERÊNCIAS
- Verruck S, Dantas A, Prudencio ES. Functionality of the components from goat’s milk, recent advances for functional dairy products development and its implications on human health. J Funct Foods. 2019;52:243–57.
- Demirci T, Sert D, Aktaş K, Atik DS, Negiş HIO, Akin N. Influence of hot and cold break tomato powders on survival of probiotic L. paracasei subsp. paracasei F19, texture profile and antioxidative activity in set-type yoghurts. Trends Food Sci Technol. 2020;118:108855.
- De La Rosa LA, Moreno-Escamilla JO, Rodrigo-García J, Alvarez-Parrilla E. Postharvest Physiology and Biochemistry of Fruits and Vegetables: Phenolic Compounds. Cambridge:Woodhead; 2019.
- Seo KH, Jeong J, Kim, H. Synergistic Effects of Heat-Killed Kefir Paraprobiotics and Flavonoid Rich Prebiotics on Western Diet-Induced Obesity. Nutrients. 2020;12:2465.
- Carocho M, Morales P, Ferreira I C F R. Antioxidants: Reviewing the chemistry, food applications, legislation and role as preservatives. Trends Food Sci Technol. 2018;71:107–20.
- Neha K, Haider MR, Pathak, Yar A MS. Medicinal prospects of antioxidants: A review. Eur J Med Chem. 2019;178:687-704.
- Shah MA, Bosco SJD, Mir SA. Plant extracts as natural antioxidants in meat and meat products. Meat Sci. 2014;98:21-33.
- Dias JL, Mazzutti S, Souza JA, Ferreira SR, Soares LA, Stragevitch L, Danielski L. (2019). Extraction of umbu (Spondias tuberosa) seed oil using CO2, ultrasound and conventional methods: Evaluations of composition profiles and antioxidant activities. J Supercrit Fluids. 2019;145:10-18.
- Vieira GS. Estudo dos processos de extração de Antocianinas da polpa de juçara (Euterpe edulis Mart.) E da concentração do extrato por nanofiltração [tese]. Campinas: Universidade Estadual de Campinas; 2015.
- Novello Z. Extração e caracterização química de extratos obtidos de matrizes vegetais utilizando n-butano pressurizado como solvente [tese]. Erechim: Universidade Regional Integrada do Alto Uruguai e das Missões; 2015.
- Oliveira VB, Zuchetto M, Oliveira CF, Paul, CS, Duarte AFS, Miguel MD, Miguel OG. Efeito de diferentes técnicas extrativas no rendimento, atividade antioxidante, doseamentos totais e no perfil por clae-dad de dicksonia sellowiana (presl.). Hook, dicksoniaceae. Rev Bras Pl Med. 2016;18:10-18.
- Ribeiro LG. Extração assistida por micro-ondas de óleo essencial de folhas de eucalipto (eucalyptus urophylla x globulus) [dissertação]. Porto Alegre: Universidade Federal do Rio Grande do Sul; 2018.
- Rifna EJ, Misra NN, Dwivedi M. Recent advances in extraction technologies for recovery of bioactive compounds derived from fruit and vegetable waste peels: A review. Crit Rev Food Sci Nut. 2021;61:1-34.
- Espinosa-Pardo FA, Nakajima VM, Macedo GA, Macedo JA, Martínez J. Extraction of phenolic compounds from dry and fermented orange pomace using supercritical CO2 and cosolvents. Food Bioprod Process. 2017;101: 1-10
- Belo YN, Al-Hamimi S, Chimuka L ,Turner C. Ultra-high pressure supercritical fluid extraction and lipid chromatography from seeds of Moringa oleifera and Moringa peregrina. Bioanal. Chem. 2019;411:3685-93.
- Gupta A, Naraniwal M, Kothari V. Modern extraction methods for preparation of bioactive plant extracts. J Appl Nat Sci. 2012;1:8-26.
- Zhang X, Han, B, Hou Z, Zhang J, Liu Z, Jiang T, HE J, Li, H. Why do co‐solvents enhance the solubility of solutes in supercritical fluids? New evidence and opinion. Eur J Chem. 2002;8: 5107-11.
- Peixoto VODS, Oliveira SL, Castelo-Branco VN, Torres AG. Baru (Dipteryx alata Vogel) Oil Extraction by Supercritical-CO2: Improved Composition by Using Water as Cosolvent. J Oleo Sci. 2022;71:201-213.
- Darae A, Ghoreishi SM, Hedayati A. Extraction of supercritical CO 2 from chlorogenic acid from sunflower seed grains (Helianthus annuus): Modeling and optimization by response surface methodology. J Supercrit Fluido. 2019;144:19-27.
- Valadez-Carmona L, Ortiz-Moreno A, Ceballos-Reyes G, Mendiola JA, Ibáñez E. Valorization of cacao pod husk through supercritical fluid extraction of phenolic compounds. J Supercrit Fluido. 2018;131:99-105.
- Luna-Guevara ML, Luna-Guevara JJ, Hernández-Carranza P, Ruíz-Espinosa H, Ochoa-Velasco CE. Studies in Natural Products Chemistry: Phenolic Compounds- A Good Choice Against Chronic Degenerative Diseases. Amsterdã: Elservier; 2018.
- Shah SR, Ukaegbu CI, Hamid H. A, Alara OR. Evaluation of antioxidant and antibacterial activities of the stems of Flammulina velutipes and Hypsizygus tessellatus (white and brown var.) extracted with different solvents. J Food Meas Charact. 2018;12:1947-61.
- Mojzer BE, Knez HM, Skerget M, Knez Z, Bren U. Polyphenols: Extraction methods, antioxidative action, bioavailability and anticarcinogenic effects. Molecules. 2016; 21:901.
- Diaz AV, García-Gimeno RM. Descriptive Food Science. London: IntechOpen; 2018.
- Amarowicz R, Pegg RB. Natural antioxidants of plant origin. Food Nutr Res. 2019;90:1-81.
- Tuladhar P, Sasidharan S, Saudagar P. Biocontrol Agents and Secondary Metabolites: Role of Phenols and Polyphenols in Plant Defense Response to Biotic and Abiotic Stresses. Cambridge: Woodhead; 2021
- Cory H, Passarelli S, Szeto J, Tamez, M, Mattei J.The role of polyphenols in human health and food systems: A mini-review. Front Nutrition. 2018;5:87.
- Sayers B, Wijeyesekera A, Gibson G. Exploring the potential of prebiotic and polyphenol-based dietary interventions for the alleviation of cognitive and gastrointestinal perturbations associated with military specific stressors. J Funct Foods. 2021;87:104753.
- Hosseini SM, Behbahani M. Enhancement of probiotics viability and lactic 53 acid production in yogurts treated with Prangos ferulaceae and Carum copticum plant extracts. Biocatal Agric Biotechnol. 2021;35:102084.
- Pimentel-Moral S, Cádiz-Gurrea M L, Rodríguez-Pérez C, Segura-Carretero A. Functional and Preservative Properties of Phytochemicals- Recent advances in extraction technologies of phytochemicals applied for the revaluation of agri-food by-products. Cambridge:Academic Press; 2020.
- Basile G, Fazio A, Iacopetta, Franchini C, Sinicropi, M. S. Pomegranate: nutraceutical with promising benefits on human health. Aplic Sci. 2020; 10:6915.
- Iacopetta D, Baldino N, Caruso A, Perri V, Lupi F R, Cindio B, Gabrielle D, Sinicropil MS. et al (Nutraceuticals Obtained by SFE-CO2 from Cladodes of Two Opuntia ficus-indica (L.) Mill Wild in Calabria. Aplic Sci. 2021;11:477.
- Renard CMGC. Extraction of bioactives from fruit and vegetables: state of the art and perspectives. Food Sci Technol.2018; 93:390-95.
- Srinivas K, King JW. Functional Food Product Development. Hoboken: Wiley-Blackwell; 2010.
- Gros Q, Duval J, West C, Lesellie E. Supercritical fluid extraction-supercritical fluid chromatography (SFE-SFC) at a glance: A coupling story. Trends Analyt Chem. 2021;144:116433.
- Meireles M A. Extracting Bioactive Compounds for Food Products: Theory and Applications. Boca Raton:CRC Press; 2008.
- Lefebvre T, Destandau E, Lesellier E. Selective extraction of bioactive compounds from plants using recent extraction techniques: A review. J Chromatog. 2021; 1635:461770.
- Garcia-Mendoza MP, Paula JT, Paviani LC, Cabral FA,Martinez-Correa HA. Extracts from mango peel by-product obtained by supercritical CO2 and pressurized solvent processes. Trends Food Sci Technol.2015;62:131-137.
- Garcia-Mendoza MP, Espinosa-Pardo F A, Baseggio A M, Barbero GF, Junior MRM, Rostagno MA, Martínez J. Extraction of phenolic compounds and anthocyanins from juçara (Euterpe edulis Mart.) residues using pressurized liquids and supercritical fluids. The J Supercrit Fluids. 2017;119:9-16.
- Cristofoli NL, Lima CAR, Vieira M M C, Andrade KS, Ferreira, SR. Antioxidant and antimicrobial potential of cajazeira leaves (Spondias mombin) extracts. Sep Sci Technol. 2019;54: 580-590.
- Martins CM, Guedes JAC, Brito ES, Ferreira SRS. Valorization of tamarind seeds using high-pressure extraction methods to obtain rich fractions in fatty acid and phenolic compounds. J Supercrit Fluids. 2022;183:105556.
- Mesquita PC, Rodrigues LGG, Mazzutti S, Silva M, Vitali L, Lanza M. (2021). Intensified green-based extraction process as a circular economy approach to recover bioactive compounds from soursop seeds (Annona muricata L.). Food chem. 2021;12:100164.
- Teixeira GL, Maciel L G, Mazzutti S, Barbi R C T, Ribani R H, Ferreira SRS, Block JM. Sequential green extractions based on supercritical carbon dioxide and pressurized ethanol for the recovery of lipids and phenolics from Pachira aquatica seeds. J Clean Prod. 2021;306:127223.
- Viganó J, Coutinho JP, Souza DS, Baroni NA, Godoy HT, Macedo JA, Martínez J. Exploring the selectivity of supercritical CO2 to obtain nonpolar fractions of passion fruit bagasse extracts. J Supercrit Fluids. 2016;110:1-10.
- Farías-Campomanes AM, Rostagno M A, Meireles MAA. Production of polyphenol extracts from grape bagasse using supercritical fluids: Yield, extract composition and economic evaluation. J Supercrit Fluids. 2013;77:70-78.
- Cavalcanti RN, Veggi PC, Meireles MAA. Supercritical fluid extraction with a modifier of antioxidant compounds from jabuticaba (Myrciaria cauliflora) byproducts: economic viability. Procedia Food Sci. 2011;1:1672-78.
- Pies G. Tecnologia supercrítica aplicada à obtenção de extratos ricos em compostos fenólicos a partir de casca de jabuticaba Plinia trunciflora (O. Berg) Kausel [tese] Florianópolis: Universidade Federal de Santa Catarina; 2017.
- Paes J, Dotta R, Barbero GF, Martínez J. Extraction of phenolic compounds and anthocyanins from blueberry (Vaccinium myrtillus L.) residues using supercritical CO2 and pressurized liquids. J Supercrit Fluids. 2014;95:8-16.
- Cerón IX, Higuita JC, Cardona, CA. Design and analysis of antioxidant compounds from Andes Berry fruits (Rubus glaucus Benth) using an enhanced-fluidity liquid extraction process with CO2 and ethanol. J Supercrit Fluids. 2012;62:96-101.
- Melo MMR, Silvestre AJD, Silva CM. Supercritical fluid extraction of vegetable matrices: Applications, trends and future perspectives of a convincing green technology. J Supercrit Fluids. 2014;92:115–176.
Tag:ENAG
