HIDROCARBONETOS POLICÍCLICOS AROMÁTICOS (HPAs) EM CAFÉ: UMA REVISÃO DE LITERATURA
Capítulo de livro publicado no livro do I Congresso Latino-Americano de Segurança de Alimentos. Para acessa-lo clique aqui.
DOI: https://doi.org/10.53934/08082023-26
Este trabalho foi escrito por:
Edilaine Alves da Silva Santos *; Lucas Caldeirão Rodrigues Miranda ;Natalia Costa da Silva Helena Teixeira Godoy
Edilaine Alves da Silva Santos – Email: [email protected]
Resumo: O café se destaca entre os produtos mais comercializados no mundo, entretanto o processamento do grão pode desencadear a formação de contaminantes, a exemplo dos hidrocarbonetos policíclicos aromáticos (HPAs). Alguns dos compostos desse grupo apresentam potencial cancerígeno, genotóxico, citototóxico portanto, faz-se necessário estudos que avaliem a presença deles em alimentos. Diante disso, o presente trabalho tem por objetivo, levantar dados a respeito da ocorrência de HPAs em café, bem como de métodos analíticos e de preparo de amostra utilizados para investigação desses compostos. Para isso foi desenvolvida uma revisão de literatura sobre o processamento do café, associando as etapas do processo com a incidência de HPAs, também um levantamento de dados sobre o as metodologias descritas para análise de HPAs em amostras de café, tendo como base 56 e artigos, de diversos países. Esse levantamento mostrou que a técnica de cromatografia a gás (GC-MS) é a mais utilizada, e para preparo de amostra são principalmente empregadas técnicas de extração em fase sólida (SPE). Também evidenciou a baixa quantidade de estudos que avaliem HPAs em cafés comerciais brasileiros.
Palavras–chave: Contaminante, Hidrocarbonetos policíclicos aromáticos, alimentos
Abstract: Coffee stands out among the most commercialized products in the world, however the processing of the grain can present the formation of contaminants, such as polycyclic aromatic hydrocarbons (PAHs). Some of the compounds in this group have carcinogenic, genotoxic, cytotoxic potential, therefore, studies are needed to assess their presence in foods. In view of this, the present work aims to collect data regarding the occurrence of PAHs in coffee, as well as analytical and sample preparation methods used to investigate these compounds. For this, a review of the literature on coffee processing was carried out, associating the process steps with the incidence of PAHs, as well as a data collection on the methodologies described for the analysis of PAHs in coffee samples, based on 56 articles from different countries. This survey showed that the gas chromatography technique (GC-MS) is the most used, and solid-phase extraction (SPE) techniques are mainly used for sample preparation. It also evidenced the low number of studies evaluating PAHs in Brazilian commercial coffees.
Keywords: Poisoning; Polycyclic aromatic hydrocarbons; foods.
- INTRODUÇÃO
No contexto mundial, o café destaca-se como uma das bebidas mais populares (1) e tem apresentado aumento no consumo. Esse fato deve-se aos benefícios associados a essa bebida, bem como ao seu aroma e sabor marcantes e agradáveis. Além disso, o café é conhecido como um estimulante (2), uma fonte de ácidos clorogênicos na dieta humana, compostos antioxidantes e outros compostos bioativos (3). Embora os benefícios do consumo de café sejam amplamente divulgados, diversos estudos têm sido conduzidos para avaliar a incidência de contaminantes nesse alimento.
A contaminação por substâncias tóxicas pode ocorrer em diferentes etapas da cadeia produtiva, desde o cultivo até o preparo para consumo. Destacam-se contaminantes naturais, como fitotoxinas e micotoxinas, e contaminantes ambientais, como bifenilas policloradas (PCBs), dioxinas. Além disso, durante o processamento do café, podem ser formados contaminantes como acrilamida, nitrosaminas, furano, cloropropanóis aminas heterocíclicas, hidrocarbonetos policíclicos aromáticos (HPAs) e agrotóxicos(4)(5)(6)(7). A etapa de torrefação é uma das fases do processamento do café, na qual ocorrem diversas reações químicas que levam à alteração dos compostos presentes nos grãos. Durante esse processo térmico, alguns compostos são degradados enquanto outros são formados. A presença de precursores nessas reações pode desencadear a formação de contaminantes, como é o caso dos HPAs (8)(9)(10). Que são compostos resultantes da combustão incompleta e pirólise da matéria orgânica (11). Eles possuem baixa afinidade com a água, baixa solubilidade e alto coeficiente de partição octanol-água (12). A presença desses compostos em alimentos é motivo de preocupação, uma vez que alguns deles são descritos como mutagênicos, carcinogênicos, genotóxicos ou citotóxicos (13).
No contexto brasileiro, a determinação dos HPAs em amostras de café nacional é de extrema importância, tendo em vista o alto consumo de café pela população. Segundo a Associação Brasileira da Indústria de Café, o Brasil ocupa a segunda posição no ranking mundial de consumo de café, e o consumo per capita nacional em 2021 foi de 4,84 kg por ano de café torrado. Portanto, é fundamental avaliar a ocorrência de HPAs em amostras de café. Tendo em vista esses fatos, ressaltando a preocupação em torno do tema, o presente trabalho tem por objetivo demonstrar como pode se dar a ocorrência de HPAs em café e realizar um levantamento de estudos que verifiquem a ocorrência de HPAs em amostras de café.
2. MATERIAL E MÉTODOS
Para o desenvolvimento do presente trabalho realizou-se um levantamento inicial, onde foram selecionados 159 trabalhos. Para essa seleção utilizou-se as palavras-chave, café e HPAs para busca, nas plataformas Science direct e Springer. Depois dessa seleção inicial realizou-se uma segunda seleção, onde os trabalhos foram lidos, e selecionou-se os que realizaram determinação de HPAs em amostras de café, sendo um total 48 artigos. Além desses trabalhos também foram lidos 56, acerca do tema para estruturar a revisão.
3. RESULTADOS E DISCUSSÃO
3.2 REVISÃO DE LITERATURA
3.2.1 Café
O café é uma bebida mundialmente conhecida e consumida, sua obtenção se dá a partir do grão do café torrado e moído. O grão do café é obtido do cafeeiro, planta a qual produz frutos arredondados semelhantes a uma cereja, quando maduros podem atingir a coloração amarela ou vermelha. O grão apresenta duas sementes semiesféricas que retiradas do fruto são denominadas de “grão de café verde”, sendo essa parte destinada ao processamento para a obtenção do café torrado e moído (14). O grão de café verde é o principal produto de interesse comercial proveniente do fruto. O grão representa cerca de 50-55% da matéria seca e apresenta variabilidade em tamanho, forma e densidade, características influenciadas por práticas agrícolas e espécie cafeeira (15).
O fruto do cafeeiro é uma drupa, sendo caracterizado como carnoso, com o pericarpo diferenciado em exocarpo, mesocarpo e endocarpo (16). O exocarpo é o tecido mais externo da estrutura do fruto, sendo uma camada de células compactadas. O tecido que compõem mesocarpo é formado por células parenquimatosas, apresenta característica de ser rígido. Já o endocarpo é a estrutura mais interna do pericarpo, formado por células esclerenquimatosas, é a parte mais próxima da semente, que é formada pela película prateada, endosperma e embrião (2). Dentre a estruturas citadas anteriormente, pode-se destacar que a composição do endosperma está associada aos compostos precursores do aroma e sabor do café torrado, sendo também o principal tecido de reserva.
Sobre este grão, historicamente indicasse a Etiópia como lugar de origem do café, sendo que relatado que se disseminou primeiro para a Índia, seguida da Indonésia, Brasil, Colômbia e América Central(16)(17).
3.2.1.1 Classificação botânica
Em relação a classificação botânica, o café pertence à família Rubiaceae, que é composta por vários gêneros, tendo destaque econômico o gênero Coffea. Dentro desse gênero são cultivadas as espécies Coffealiberica (café Libérica), Coffeadewevrei (café Excelsa), Coffea arabica (café Arábica) e Coffea canephora (café Robusta), onde as duas últimas apresentam grande relevância na economia mundial correspondendo a mais de 60% da produção, sendo importante destacar que a produção de café comercial geralmente tem como base o blend dessas duas espécies, de acordo com Organização Internacional do Café.
O Coffea arábica é conhecido por sua fragilidade em comparação com robusta, as plantas têm melhor cultivo em clima temperado (19-22°C), têm a forma de um elipsóide semi-triaxial com uma fenda longitudinal sigmoidal em seu lado plano (15). Essa espécie requerer um manejo agronômico mais cuidadoso em termos de nutrição, fitossanidade (pragas e doenças), colheita, e pós-colheita (18). Apresentando um preço mais alto no mercado internacional (19). O Coffea arábiaca possuí em sua composição 0,8-1,4% de caféina, 7-9% de ácido clorogênico e 0,6-1,2% de trigonelina. Já o Coffea canéfora apresenta em sua composição 1,7-4% de cafeína, 7-12% de ácido clorogênico e 0,3-0,9% de trigonelina (20). As espécies apresentam características distintas em sua composição em decorrência das diferentes condições aplicadas para seu manejo e cultivo. O Coffea canéfora ocupam preferencialmente as zonas equatoriais de baixa altitude, caracterizam-se como plantas mais vigorosas, os grãos são mais redondos com uma fenda central ligeiramente reta(15), e são menos suscetíveis a ataques de doenças (18)(Luis et al., 2020).
3.2.1.2 Composição físico-química café verde
As substâncias presentes no grão do café podem ser classificadas de acordo com a afinidade pela água. As substâncias hidrossolúveis são a cafeína, trigonelina, ácido nicotínico, ácidos clorogênicos, mono, di e oligossacarídeos, algumas proteínas, minerais e ácidos carboxílicos. Os compostos insolúveis mais encontrados em maior proporção são celulose, lignina, hemicelulose, lipídios, proteínas e minerais (16).
A composição do café verde inclui inúmeros compostos, podendo-se citar os polissacarídeos, que ficam localizados na parede celular (50%), celulose (15%), arabinogalactana-proteinas (25 a 30%), mananas ou galactomananas (50%) e pectina (5%) (16) (21) (22). Dentre os compostos, alguns apresentam funções primordiais no grão, sendo estes a arabinogalactana, a qual tem a função de agregar os componentes químicos da parede celular; a manana considerada um polissacarídeo de reserva com função de estruturar a parede das células do grão de café; e a celulose que constitui o esqueleto da parede celular da semente. Vale ressaltar que, a sacarose é o carboidrato de baixo peso molecular predominante no café cru (23)(24). Os carboidratos presentes no grão de café são compostos extremamente importantes, pois tem influência no aroma, na estabilidade da espuma, bem como na viscosidade (2).
Além do grupo dos carboidratos, os lipídeos e as proteínas são substâncias presentes em quantidades representativas no grão. Dentre a fração lipídica estão presentes cera, triglicerídeos, ésteres de álcoois diterpênicos, ácidos graxos, álcoois diterpênicos, esteróis, tocoferóis, fosfatideos e ácidos graxos livre esterificado na forma de triacilgliceróis (25). Já as proteínas podem ser encontradas na semente do café em suas formas solúveis ou insolúveis, também como aminoácidos livres e peptídeos (26).
Outros compostos importantes também são encontrados, a exemplo dos ácidos clorogênicos, onde o ácido cafeico, ferúlico e p-cumárico apresentam maior importância em termos de quantidade (27). A cafeína é uma substância de grande destaque em relação a composição do café, encontrando-se livre no citoplasma e ligada a parede celular podendo estar associada a ácidos clorogênicos. Também há presença de trigonelina, ácido nicotínico, outros ácidos carboxílicos (acético, cítrico, málico, fórmico, químico, succínico), bem como os minerais que correspondem a 4% da massa seca do café cru, tendo destaque potássio, magnésio, fosforo e cálcio (16).
A cafeína é um alcalóide de grande importância para o café, estando diretamente associado à qualidade das bebidas de café, já que tem relação direta com o amargor (28). É reconhecida pela sua ação estimulante no sistema nervoso central, aumento do estado de alerta, circulação sanguínea e respiração (29). Outros possíveis benefícios da cafeína incluem a melhora do humor e o melhor desempenho em exercícios, sendo um dos fatores que trazem destaque e tem influência sobre a grande aceitação da bebida (30). Embora os benefícios, o consumo de cafeína foi associado a insônia e dependência leve, em altas doses a cafeína foi vinculada a ansiedade, inquietação, tensão, nervosismo e agitação psicomotora (31).
3.2.1.3 Mercado do café
O café se destaca como uma das bebidas mais consumidas em escala mundial. Segundo a Instrução Normativa nº 16, de 24 de maio de 2010, entende-se por café (bebida), o líquido obtido por infusão, percolação, decantação ou outro processo de preparo a partir do café torrado e moído. Apesar de haver diferentes espécies de café, maior parte da bebida café é obtida a partir das espécies Coffea arabica (Arabica) e Coffea canephora (Robusta). O café arábica se destaca por suas propriedades sensoriais, é uma bebida de aroma e sabor refinado, enquanto o café robusta é descrito como um café neutro, de sabor fraco, destacando o amargor (1).
O café é reconhecido comercialmente como commodity agrícola, tendo grande destaque no cenário mundial. Segundo dados da Organização Internacional do Café, aproximadamente 170 países produzem café, tendo destaque o Brasil, Vietnã, Colômbia e Indonésia. Nesse cenário o Brasil também se destaca como maior exportador desse produto. E com relação ao consumo estima-se que o café seja uma das bebidas mais consumidas em todo o mundo (32).
A popularidade desta bebida está associada ao aroma e sabor marcante e agradável, bem como as suas propriedades. A infusão do café é conhecida como estimulante, propriedade atribuída principalmente à cafeína (Esquivel & Jiménez, 2012). Além da cafeína outros compostos presentes no café apresentam efeito positivo sobre a saúde, como ácido clorogênico, ácido nicotínico, trigonelina, ácido quinolínico, ácido taninico, ácido pirogolico (Minamisawa et al., 2004). O café reconhecido como principal fonte de ácido clorogênico da dieta humana, sendo também uma fonte compostos de antioxidantes e outros compostos bioativos (Farah, 2012).
Essa notoriedade dos benefícios do café vem contribuindo com o aumento do consumo por parte da população mundial, a acessibilidade da bebida para qualquer população social e econômica, é um fator que também contribui, bem como os hábitos gerados em torno dessa bebida, como pausa durante o trabalho exaustivo ou dias de estudo, e a necessidade contemporânea de conveniência, espaços de interação social e para simplesmente desfrutar, as cafeterias apresentam um fenômeno relevante em todas as cidades urbanas ao redor do mundo. Em função da demanda durante todos os períodos do ano e por ser sazonal o armazenamento é necessário para manter a melhor qualidade. Nesse sentido, vários países tropicais e subtropicais produzem café extensivamente (33).
3.2.2 Processamento
O processamento para obtenção do café torrado e moído engloba etapas, iniciando com a colheita. A colheita do café pode ser realizada tanto manualmente quanto mecanicamente. A colheita manual confere maior seletividade ao colher frutos em diferentes estádios de maturação, uma vez que no mesmo pé ou até no mesmo galho pode haver frutos com graus de maturação diferentes, pois os frutos do cafeeiro geralmente não amadurecem de forma simultânea. Sendo importante ressaltar que frutos fora do estádio de maturação tido como o ideal (maduro) podem desencadear formação de defeitos no produto. Apesar de uma boa seletividade dos frutos, esse processo acaba sendo demorado e, portanto, caro. A colheita mecânica é realizada agitando as árvores, ou com equipamentos que funcionam como um “pente flexível” retirando os frutos dos galhos, que ao contrário do outro método, não há seletividade do grão, o que pode ocasionar presença de sujidades, como pedras, galhos, folhas, bem como defeitos de rendimento, frutos não maduros, frutos fermentados ou até mesmo frutos na senescência. No entanto, apresenta um valor menor que a colheita manual(34).
Após a colheita, não é indicado que fruto seja armazenado por longos períodos, pois há risco de fermentação, contaminação microbiana, inclusive por fungos toxicogênicos, podendo também haver a formação de defeitos (16).
3.2.2.1 Processamento primário
O processamento do fruto do café até a obtenção do café torrado moído é composto por várias etapas. Como a recepção que ocorre em moegas, abanação que objetiva a separação de impurezas dos frutos e pode ser realizada de forma manual ou mecânica, na sequência ocorre a separação hidráulica dos frutos, a qual ocorre em lavadores, por meio da diferença de densidade, separando em dois grupos, frutos verdes ou mais densos, e dos menos densos, chamados de boia (3). Em seguida a extração da polpa, nessa etapa ocorre a produção do grão de café verde. Esse processo de extração pode ocorrer por via seca e a via úmida. A Figura 1 esboça um fluxograma de processamento primário do café.
Na via seca os frutos são processados na sua forma integral, as sementes são expostas ao sol ou secadores de ar até que o teor de umidade seja de aproximadamente 10%-12% (34). Logo após o processo de secagem, a casca e a polpa dos grãos são removidas. O exocarpo que originalmente é amarelo ou vermelho torna-se escuro, há diminuição do tamanho da cereja em até 40%, formando o café coco ou café natural. Sendo importante ressaltar que no Brasil o café é normalmente produzido por via seca, e que essa forma de beneficiamento apresenta menor geração de resíduo sólidos e líquidos (16).
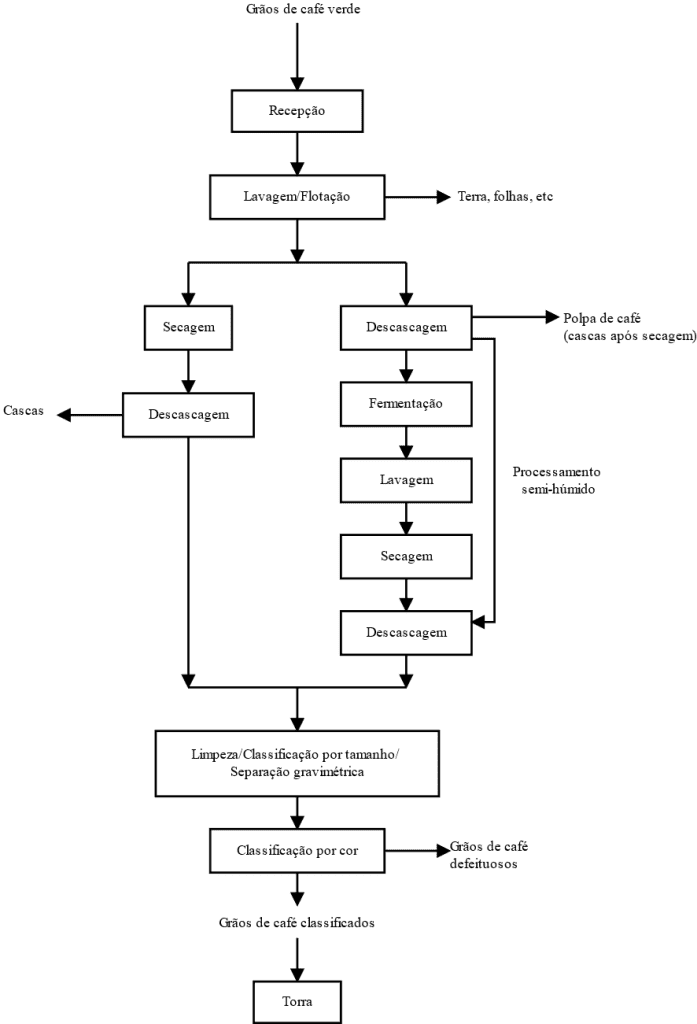
Figura 1. Processamento primário do café (Adaptado de Franca, Oliveira, 2019).
Por outro lado, na via úmida são produzidos os cafés pergaminhos (2). É possível obter três formas de café no processado por via úmida, o café despolpado, obtido pela remoção mecânica da casa e a mucilagem por fermentação biológica, o descascado, com remoção da casca e parte da mucilagem mecanicamente e o desmucilado, obtido removendo mecanicamente toda a casca e a mucilagem (16). O descascamento é uma etapa comum a todos as formas de processamento por via úmida, a quantidade de frutos verdes é um fator que pode comprometer essa etapa. Em seguida ocorre despolpamento, onde o café descascado é direcionado para tanques de fermentação, por um período de 12 a 48 horas. Essa etapa objetiva a hidrólise da mucilagem. Após a fermentação o café deve ser lavado manual ou mecanicamente para finalizara remoção da mucilagem e, em seguida, podem ser secos ao sol ou em secadores de ar e armazenados para uso comercial, bem como na via seca (35).
Logo após a secagem dos grãos, por via seca ou via úmida ocorre a cura, que é a retirada da casca e o armazenamento(36) . Nesta etapa ocorre limpeza granulometria e por densidade, triagem colorimétrica e ensacamento em sacos padrão de 60kg. Depois desse primeiro tratamento realizado, os grãos podem ser comercializados para serem processados, seguindo etapas de torrefação e moagem (16).
3.2.2.2 Torrefação
Depois da etapa de secagem o café pode ser armazenado ou direcionado para o processamento visando a obtenção de um produto. Nesse sentido é importante destacar a torrefação como uma das principais etapas do processamento, visto que essa etapa é responsável pela conversão do grão do café verde em café torrado. A torrefação é um tratamento térmico a seco, onde os grãos são expostos ao ar quente, havendo o aumento da temperatura, que desencadeia reações químicas, desidratação, e alterações na microestrutura(37). A torrefação do café requer temperaturas elevadas e superiores a 190° C, para possibilitar o desenvolvimento das características sensoriais desejadas (3).
O calor transferido para o café verde tem grande influência sobre as transformações que ocorrem no grão, onde a etapa de torra pode ser dividida em três etapas, sendo inicialmente na torrefação, na qual ocorre a evaporação da água livre. Nesta fase quando a temperatura das sementes atinge 130° C, a sacarose carameliza, e as sementes começam a apresentar coloração dourada e inchar, sendo possível observar também o desaparecimento do cheiro de café verde (14), onde as alterações químicas nesta fase inicial são pequenas em relação as outras fases da torrefação. Ao atingir temperaturas superiores a 160° C, iniciam-se uma série de reações, onde a composição química dos grãos muda drasticamente, ocorrendo desprendimentos em grandes quantidades de moléculas de dióxido de carbono. É perceptível a mudança na coloração das sementes para marrom claro, o aumento do volume e o início da formação de aroma (3). Em temperaturas superiores a 190° C, é possível observar as reações de Maillard e Strecker, que envolvem carboidratos, proteínas e outras classes de compostos de baixo e alto peso molecular (37). Ao atingir a temperatura desejada, pelo período ideal o processo é interrompido e as sementes são rapidamente resfriadas pelo uso de água ou ar, sendo preferível o emprego do ar. Esse tratamento térmico pode durar em período de 3 a 20 minutos (3).
A temperatura nessa fase tem correlação com alguns parâmetros, como a cor, onde quanto maior a temperatura, mais escuro o café, podendo classificar em graus de torra, “leve”, “médio” ou “escuro”. O aumento da temperatura durante a torrefação é constante até atingir a temperatura máxima que pode variar de 200 a 250° C (37). As temperaturas empregadas na torra podem estar relacionadas ao tipo de torrefador utilizado, geralmente em torrefadores de cama de fluidos as temperaturas podem atingir até 250° C (3). Bem como o tempo, que influencia as reações, períodos de torra mais longos podem gerar um café amargo e sem o aroma desejado, já períodos de torra curtos podem ser insuficientes para que todas as reações ocorram (37).
Comumente o processo descontínuo para torrefação do café é o que mais ocorre, resumidamente nesse processo os grãos são carregados em cilindros horizontais rotativos, onde o ar quente é soprado para dentro para aquecer os grãos, por temperaturas em torno de 220° C, por um período suficiente para atingir o grau de torra desejado. Com relação ao grau de torra, geralmente é avaliado por medições de refletância de luz de grãos torrados moídos ou inspeção visual de sua cor por um operador (38).
Na torrefação algumas alterações são evidenciadas, em função da sucessão de reações que provocam modificações na composição do grão de café. Essa etapa é considerada como determinante, pois nela ocorre a formação de propriedades físicas, que tem influência direta nas características sensoriais, tecnológicas e funcionais do café (37). Em virtude da formação de compostos relacionados ao sabor e aroma característico da bebida, desenvolvimento da coloração escura, textura porosa e quebradiça que favorece a moagem (14). Outros fatores também podem ser observados, como aumento do volume, a estrutura se torna mais porosa (39) grão, bem como vaporização da água e conversão de matéria seca em compostos voláteis (37). Dentre algumas das reações que ocorrem durante a torrefação, tem a formação carboidratos de baixo peso molecular, a partir de polissacarídeos (40), alteração da coloração em função da pirólise de compostos orgânicos (20). E outras reações, como reação de Maillard, degradação de Strecker, pirólise, caramelização, desnaturação e degradação de proteínas e de alguns ácidos (41).
Após a torrefação do café, há uma alteração da composição em decorrência das reações ocorridas durante o processamento, nessa fase do processo encontram-se os seguintes compostos e suas respectivas concentrações carboidratos (38–42% base seca), melanoidinas (23%), lipídios (11–17%), proteínas (10%), minerais (4,5–4,7%), ácidos clorogênicos (2,7–3,1%), ácidos alifáticos (2,4–2,5%), cafeína (1,3–2,4%), dentre outros em menor concentração (20). O grão do café é, então, moído, podendo ser comercializado como café torrado moído ou podem ser direcionados para fabricação de café instantâneo (3).
Sendo importante destacar a relação da qualidade sensorial do café e a etapa de torrefação. Os atributos sensoriais que indicam qualidade do café, compreendem aroma, acidez, amargor, corpo, sabor e impressão global da bebida. A intensidade e equilíbrio desses parâmetros definem a qualidade sensorial do café (42). Sabe-se que esses parâmetros são influenciados diretamente pelas espécies utilizadas, manejo e condições de cultivo das plantas, grau de maturação na colheita, método de colheita e método do processamento.
3.2.3 Hidrocarbonetos policíclicos aromáticos (HPAs)
Os hidrocarbonetos policíclicos aromáticos (HPAs) se referem a um grupo formado por mais de 200 compostos orgânicos, em sua estrutura apresentam dois ou mais anéis aromáticos fundidos (43). Como características, destaca-se a alta hidrofobicidade, baixa solubilidade em água, alto coeficiente de partição octanol-água, baixa pressão de vapor e altos pontos de fusão e ebulição, dependendo das estruturas (12). Tais propriedades torna-os mais persistentes no ambiente (44) . Outro ponto importante sobre as características dessas substâncias, é que há HPAs de baixo peso molecular, estes são formados por três ou menos anéis aromáticos, já os de alto peso molecular, são moléculas que em sua estrutura apresentam quatro ou mais anéis aromáticos (11).
Esses compostos são formados principalmente como resultado da combustão incompleta e pirólise da matéria orgânica, sendo contaminantes ambientais que podem estar presente em qualquer meio devido a deposição desses compostos na atmosfera, pela ocorrência incêndios florestais, erupções vulcânicas, emissão de gases e partículas de veículos motorizados e indústrias, derramamentos de óleo, sistemas de aquecimento doméstico, usinas de energia, combustíveis fósseis, refino de petróleo, gaseificação de carvão e incineração de resíduos. Tais fatores e as características dos HPAs possibilitam a bioacumulação destes no meio ambiente (45); (11); (46).
O contato dos seres humanos com os HPAs está associado a três principais vias, ingestão, respiração e o contato dérmico. O consumo de alimentos é uma via importante para a exposição humana a contaminantes ambientais (47). Estudos tem evidenciado que a contaminação de alimentos por esses compostos podem ser a partir de fontes ambientais, processamento de alimentos industriais e de preparação de alimentos domésticos (48).
A ocorrência dessas substâncias em alimentos deve-se ao preparo, processamento de alimentos ou até mesmo pela entrada na cadeia produtiva de alimentos quando culturas ou plantas são cultivadas com recursos contaminados, como solo, ar ou água (49). Tecnologias de processamento que envolvam altas temperaturas, como secar, assar ou grelhar são indicadas como possíveis fontes de formação de contaminantes como HPAs (50). Nos últimos anos estudos vêm sendo realizados para determinar os níveis de exposição a HPAs, e alimentos como cereais, carnes, gorduras e óleos demonstram níveis significativos desses compostos quando estes são defumados e grelhados (49). Processos de torrefação e secagem de grãos de café, grãos de cacau e folhas de chá podem contribuir para o aumento do teor de HPAs (51), principalmente quando estes passam por processos excessivos em relação a temperatura e tempo de exposição a temperatura elevadas (52).
A formação dos HPAs no café ocorre pela pirólise de compostos presentes nessa matriz, durante a etapa de torrefação. Em função da complexidade da composição do café é difícil descrever as reações envolvidas na formação desses compostos com precisão (53). Sob altas temperaturas ocorre a quebra de macromoléculas (carboidratos, lipídeos e proteínas), podendo acarretar a formação de moléculas mais leves de baixo peso molecular e radicais livres intermediários, que apresentam alta reatividade (47); (54). Quando estes compostos são ciclicizados e recombinados podem formar compostos de alto peso molecular a exemplo dos HPAs (55). Essas moléculas migram gradualmente para a parte hidrofóbica do alimento e se acumulam (56).
Em um estudo realizado por (57) sobre mecanismos para formação de HPAs, são sugeridas três vias de formação desses compostos, sendo essas, com adições de acetileno, mecanismo Diels-Alder e mecanismo de formação com radicais, mas nenhuma das vias é diretamente indicada como principal via para formação desses compostos em alimentos.
A exposição aos HPAs pode estar associada a efeitos adversos, como interferência na função normal das membranas celulares e sistemas enzimáticos (58). A toxicidade dos HAPs pode induzir sintomas como vômitos, náuseas, diarreia, inflamação e vermelhidão da pele, danos nos rins e fígado, diminuição da imunidade ou imunossupressão, ruptura de células sanguíneas, deficiências congênitas, doenças mediadas por estresse oxidativo, toxicidade genética, transformação celular e carcinogenicidade (59); (60); (61); (62); (63); (64). Os efeitos tóxicos associados a exposição aos HPAs são separados em efeitos agudos e efeitos crônicos. Estudos destacam que os efeitos agudos promovidos pelos HPAs dependem do tempo, da via de exposição, número ou concentração de exposição, do nível de toxicidade do composto, estado de saúde e idade (65);(61);(66). O impacto da exposição a curto prazo dos HPAs não é claro, já a exposição ocupacional, a longo prazo a poluentes mistos contendo altas concentrações de HPAs, pode causar sensibilidade ocular, irritação, náusea, vômito, diarreia, confusão, irritação e inflamação da pele (67), podendo-se citar o antraceno e benzo(a)pireno como irritantes diretos da pele que podem causar reações alérgicas cutâneas em animais e humanos (68); (52). Estudos indicam que alguns desses compostos são relacionados a teratogenicidade (69); (70); (62); (71); (64), genotoxidade (72); (73); (74), imunotoxicidade (75), carcinogênese e efeitos citotóxicos (13). A carcinogenicidade desses compostos pode variar de acordo com o número e estrutura dos anéis aromáticos que compõem a molécula (76).
Após entrar no organismo, em função da sua lipofilicidade, os HPAs são facilmente absorvidos (77); (67). Boa parte dos contaminantes desse grupo são ingeridos junto com alimentos, passam pelo trato gastrointestinal, seguem absorvidos pelo metalismo de primeira passagem e, então, no fígado, passam pela biotransformação (78). Normalmente os HPAs não apresentam características eletrofílicas, que permitem a ocorrência de interações covalentes com os centros nucleófilos do DNA e outras moléculas. Entretanto, quando ocorre conversão metabólica dos HPAs, por sistemas microssômicos oxidativos, são formados intermediários (epóxidos e diol epóxidos) capazes de gerar espécies de carbocátions altamente reativas que, por sua vez, estão associados com a ligação com o DNA. Essa ativação ocorre por meio de enzimas do citocromo P450(79); (63). Os produtos de adição formados causam uma distorção na estrutura de dupla hélice do DNA, comprometendo sua função e induzindo o desenvolvimento de aduto, e consequentemente alteração genética, erros e mutações na replicação do DNA (43), porém os organismos possuem mecanismo de reparo para eliminação de adutos de DNA, por meio da excisão de nucleotídeos (80). Caso esses adutos não sejam reparados, podem causar mutações permanentes (81), podendo ser pior se esses metabolitos estiverem em locais críticos com genes supressores de tumor ou oncogenes, pois podem iniciar o processo de carcinogênese (82).
A atividade carcinogênica do BaP, por exemplo, é resultado de sua biotransformação. No fígado esse composto é oxidado formando o BaP-7,8-dihidrodiol-9,10-epóxido, que pode se ligar ao DNA modificando o mecanismo de replicação(83); (84). Para esclarecer mais esse processo, sabe-se que a estrutura dos HPAs não apresenta características eletrofílicas, entretanto quando ocorre conversão metabólica desses compostos por sistemas oxidativos, podem ser formados intermediários eletrofílicos, capazes de reagir com DNA. Os produtos dessa reação têm o potencial de causar uma distorção na estrutura de dupla hélice do DNA, o que irá comprometer sua função, promovendo o travamento do aduto em uma alteração genética(43).
Diante da incidência desses compostos em alimentos e o risco associado, pode-se destacar o benzo(a)Pireno (BaP), benz(a)Antraceno (BaA), benzo(b)Fluoranteno (BbF) e Criseno (CHR), conhecido como grupo dos 4HPA, bem como a soma de 8 HPAs (os 4HPA juntamente com o benzo[k]fluoranteno [BkF], Dibenzo[ah]antraceno (DB(a,h)A), benzo [g,h, i]perileno B(g,h,i)P e indeno[1,2,3-c,d]pireno (I(c,d)P)) são compostos a serem monitorados. Esses grupos foram estabelecidos pelo Painel da Autoridade Europeia para a Segurança dos Alimentos (EFSA), como sendo indicador adequado de HPA em alimentos (48).
A Agência Internacional de Pesquisa sobre o Câncer (IARC) classifica os compostos em grupos, sendo esses: Grupo 1 – carcinogênico para humanos; Grupo 2A – provavelmente carcinogênico para humanos; Grupo 2B – possivelmente carcinogênico para humanos; Grupo 3 – não classificável quanto à sua carcinogenicidade para humanos e Grupo 4 – provavelmente não carcinogênico para humanos. Nesse sentido, é importante ressaltar que a Agência Internacional de Pesquisa sobre o Câncer (IARC) classificou alguns compostos do grupo dos HPAs, como o benzo(a)Pireno em carcinógeno humano (Grupo 1), bem como o naftaleno e o criseno, que foram considerados possivelmente cancerígenos para humanos (Grupo 2B).
Nesse sentido, o estudo desses compostos em alimentos é de suma importância, verificar níveis, processos associados e com isso tentar mensurar o risco associado a exposição a esses compostos. Segundo dados da Autoridade Europeia para a Segurança dos Alimentos (EFSA), os cereais e os frutos do mar são as classes de alimentos que mais contribuem para exposição dietética aos HPAs(48). Com isso foi determinado o limite máximo de 1 μg kg-1 de benzo(a) pireno ou sua soma com benzo(a)antraceno, criseno e benzo(b)fluoranteno em alimentos infantis, para óleos e gorduras não deve exceder 10 μg/kg, para grãos de cacau e produtos derivados 35 μg/kg, e para carnes e produtos da pesca 30 μg/kg (85)(European Commission, 2011). Sendo importante ressaltar que não há legislação que estabeleça limites para HPAs em café.
3.2.4 Metodologias para análise de HPAs em café
3.2.4.1 Técnicas Analíticas
A avaliação de contaminantes em matrizes alimentares vem sendo realizada para o monitoramento desses compostos, possibilitando a verificação da concordância com os limites máximos de resíduos permitidos para liberação de moléculas alvo, que podem estar presentes em níveis traços. Dessa maneira o uso de técnicas seletivas, com boa capacidade de separação são imprescindíveis. Nesse sentido, a cromatografia é a técnica analítica mais citada na literatura para análise de HPAs, acoplada a detectores apropriados podem reduzir o efeito de interferentes presentes nos alimentos. Para análise de HPAs em matrizes alimentares a Cromatografia Gasosa (GC) acoplada à espectrometria de massa (MS) é uma das técnicas mais citadas (50). Para análise de HPAs em café junto com GC-MS a cromatografia líquida de alta eficiência (HPLC) usando detecção de fluorescência (FLD) é uma das mais reportadas na literatura (86); (87).
3.2.4.2 Técnicas de preparo de amostra
O uso dessas técnicas analíticas requer um preparo de amostra, idealmente este deve englobar extração e limpeza, possibilitando a diminuição do efeito matriz. Atualmente técnicas de preparo de amostra como QuEChERS (Quick, Easy, Cheap, Effective, Rugged and safe), MSPE (Extração em Fase Sólida Magnética), LLE (Extração Liquido-Liquido), SPE (Extração em fase solida), tem sido utilizadas para análise de HPAs em amostras café em diversos estudos (88); (89); (90); (91).
Sobre o levantamento realizado com trabalhos que avaliaram HPAs em amostras foi perceptível que das técnicas mais citadas na literatura, GC-MS é a mais reportada para análise de HPAs. Esse fato está associado as características dos HPAs, que são moléculas volatilizáveis, bem como a sensibilidade apresentada pela técnica e seletividade do espectrômetro de massas que possibilita a confirmação da identidade da molécula através do espectro de massas. A segunda técnica mais reportada nos trabalhos é o HPLC-FLD, outras técnicas também vêm sendo utilizadas como, CG-FID, GC-SIM-MS, GC-IDMS, GC-NPD, GC-MSD, HPLC-FD, UHPLC-UV, HPLC-DAD, LC-MS, SFC-APCI-MS, RP-HPLC e HPLC -UV-VIS.
Para as técnicas de preparo de amostra a extração em fase solida (SPE) é bastante utilizada, bem como variações dessa técnica como a Extração em fase sólida magnética (MSPE) e a Microextração em Fase Solida (µ-SPE). A extração líquido-líquido também é reportada em vários trabalhos, bem como QuEChERS e Microextração Líquido-Líquido Dispersiva (DLLME).
Por meio desse levantamento foi possível perceber que há muitos estudos sobre a incidência de HPAs em amostras de café, esses trabalhos avaliaram o grão do café verde, grão torrado e moído e a bebida de café, e foram desenvolvidos em diversos países, tendo destaque China, Japão, Tailândia, Etiópia. No Brasil não há muitos estudos realizados em amostras de café comercial, sendo um ponto que chama atenção em virtude da representatividade dessa commodity em nosso território.
CONCLUSÕES
Na literatura diversos trabalhos que avaliam a presença de HPAs em amostra de café torrado evidenciam a contaminação das amostras frente ao processo de obtenção do produto comercial. Contudo, no Brasil não são apresentados dados suficientes para as amostras comercializadas em território nacional, em contrapartida o Brasil é considerado o principal exportador de café e segundo maior consumidor a nível mundial, o que reforça a importância de estudos e levantamento de dados relacionados a esse nível de contaminação. A geração de dados que demonstrem a incidência de HPAs em amostras de café produzidos e comercializados no Brasil torna-se essencial. Para isso é indispensável o desenvolvimento de técnicas analíticas e métodos de preparo e extração eficientes.
REFERÊNCIAS
- Bertrand B, Guyot B, Anthony F, Lashermes P. Impact of the Coffea canephora gene introgression on beverage quality of C . arabica. 2003;387–94.
- Esquivel P, Jiménez VM. Functional properties of coffee and coffee by-products ☆. FRIN [Internet]. 2012;46(2):488–95. Available from: http://dx.doi.org/10.1016/j.foodres.2011.05.028
- Farah A. 2 Coffee Constituents. 2012;
- Arcila A, Benavides P. Determinación de trazas de pesticidas en la producción de café en colombia. Rev Cenicafé [Internet]. 2019;70(ISSN-0120-0275):8–9. Available from: https://www.cenicafe.org/es/publications/Revista70%282%29-Web.pdf#page=6
- Barrios-Rodríguez YF, Gutiérrez-Guzmán N, Pedreschi F, Mariotti-Celis MS. Rational design of technologies for the mitigation of neo-formed contaminants in roasted coffee. Trends Food Sci Technol. 2022;120(August 2021):223–35.
- Mokhtarian M, Tavakolipour H, Bagheri F, Oliveira CAF, Corassin CH, Khaneghah AM. Aflatoxin B1 in the Iranian pistachio nut and decontamination methods: A systematic review. Qual Assur Saf Crop Foods. 2020;12(4):15–25.
- Maziero MT, Bersot LS. Micotoxinas Em Alimentos Produzidos No Brasil. Rev Bras Prod Agroindustriais. 2010;12(1):89–99.
- Chu Y-F. Coffee: emerging health effects and disease prevention. Vol. 59. John Wiley \& Sons; 2012.
- da Silva CQ, Fernandes A da S, Teixeira GF, França RJ, Marques MR da C, Felzenszwalb I, et al. Risk assessment of coffees of different qualities and degrees of roasting. Food Res Int. 2021;141(March 2020).
- Javed F, Shahbaz HM, Nawaz A, Olaimat AN, Stratakos AC, Wahyono A, et al. Formation of furan in baby food products: Identification and technical challenges. Compr Rev Food Sci Food Saf. 2021;
- Premnath N, Mohanrasu K, Raj RG, Dinesh GH, Prakash GS, Ananthi V, et al. Chemosphere A crucial review on polycyclic aromatic Hydrocarbons – Environmental occurrence and strategies for microbial degradation. Chemosphere [Internet]. 2021;280(March):130608. Available from: https://doi.org/10.1016/j.chemosphere.2021.130608
- Lee B-K, Vu VT. Sources, Distribution and Toxicity of Polycyclic Aromatic Hydrocarbons (PAHs) in Particulate Matter 99 X Sources, Distribution and Toxicity of Polycyclic Aromatic Hydrocarbons (PAHs) in Particulate Matter [Internet]. 2010. Available from: www.intechopen.com
- Armstrong B, Hutchinson E, Unwin J, Fletcher T. Lung cancer risk after exposure to polycyclic aromatic hydrocarbons: A review and meta-analysis. Vol. 112, Environmental Health Perspectives. Public Health Services, US Dept of Health and Human Services; 2004. p. 970–8.
- Buffo RA, Cardelli-freire C. Coffee flavour : an overview. 2004;(February):99–104.
- Franca AS, Oliveira LS. Coffee. In: Integrated Processing Technologies for Food and Agricultural By-Products. Elsevier; 2019. p. 413–38.
- Borém FM. Pós-Colheita do Café. UFLA; 2008.
- Illy A, Viani R. Espresso coffee: the chemistry of quality. 1995;
- Luis C, Vegro R, Almeida LF De. Global coffee market : Socio-economic and cultural dynamics [Internet]. Coffee Consumption and Coffee Industry Strategies in Brazil. Elsevier Inc.; 2020. 3–19 p. Available from: https://doi.org/10.1016/B978-0-12-814721-4.00001-9
- Gielissen R, Graafland J. Concepts of price fairness : empirical research into the Dutch coffee market. 2009;18(2):165–78.
- Belitz H-D, Grosch W, Schieberle P. Coffee, tea, cocoa. Food Chem. 2009;938–70.
- Navarini L, Gilli R, Gombac V, Abatangelo A, Bosco M, Toffanin R. Polysaccharides from hot water extracts of roasted Coffea arabica beans: isolation and characterization. Carbohydr Polym. 1999;40(1):71–81.
- Redgwell RJ, Trovato V, Curti D, Fischer M. Effect of roasting on degradation and structural features of polysaccharides in Arabica coffee beans. Carbohydr Res. 2002;337(5):421–31.
- Rogers WJ, Michaux S, Bastin M, Bucheli P. Changes to the content of sugars, sugar alcohols, myo-inositol, carboxylic acids and inorganic anions in developing grains from different varieties of Robusta (Coffea canephora) and Arabica (C. arabica) coffees. Plant Sci. 1999;149(2):115–23.
- Silwar R, Lullmann C. The determination of mono-and disaccharides in green Arabica and Robusta coffees using high performance liquid chromatography. Café Cacao Thé. 1988;
- Speer K, Kölling-Speer I. The lipid fraction of the coffee bean. Brazilian J Plant Physiol. 2006;18:201–16.
- Mazzafera P, Robinson SP. Characterization of polyphenol oxidase in coffee. Phytochemistry. 2000;55(4):285–96.
- Clifford MN, Johnston KL, Knight S, Kuhnert N. Hierarchical scheme for LC-MS n identification of chlorogenic acids. J Agric Food Chem. 2003;51(10):2900–11.
- Farah A, Monteiro MC, Calado V, Franca AS, Trugo LC. Correlation between cup quality and chemical attributes of Brazilian coffee. Food Chem. 2006;98(2):373–80.
- Belay A, Ture K, Redi M, Asfaw A. Food Chemistry Measurement of caffeine in coffee beans with UV / vis spectrometer. 2008;108:310–5.
- Heckman MA, Weil J, De Mejia EG. Caffeine (1, 3, 7-trimethylxanthine) in foods: a comprehensive review on consumption, functionality, safety, and regulatory matters. J Food Sci. 2010;75(3):R77–R87.
- Daly JW, Fredholm BB. Caffeine ᎏ an atypical drug of dependence. 1998;
- Tommerdahl KL, Hu EA, Selvin E, Steffen LM, Coresh J, Grams ME, et al. Coffee Consumption May Mitigate the Risk From the Atherosclerosis Risk in Communities Study. Kidney Int Reports [Internet]. 2022;7(7):1665–72. Available from: https://doi.org/10.1016/j.ekir.2022.04.091
- Ghosh P, Venkatachalapathy N. Processing and drying of coffee–a review. Int J Eng Res Technol. 2014;3(12):784–94.
- Toci A, Farah A, Carlos Trugo L. EFEITO DO PROCESSO DE DESCAFEÍNAÇÃO COM DICLOROMETANO SOBRE A COMPOSIÇÃO QUÍMICA DOS CAFÉS ARÁBICA E ROBUSTA ANTES E APÓS A TORRAÇÃO. Vol. 29, Quim. Nova. 2006.
- Pereira GVDM, Neto DPDC, Júnior AIM, Vásquez ZS, Medeiros ABP, Vandenberghe LPS, et al. Exploring the impacts of postharvest processing on the aroma formation of co ff ee beans – A review. Food Chem [Internet]. 2019;272(August 2018):441–52. Available from: https://doi.org/10.1016/j.foodchem.2018.08.061
- Vincent JC. Green coffee processing. In: Coffee. Springer; 1987. p. 1–33.
- Schenker S, Rothgeb T. The Roast d Creating the Beans ’ Signature. 2017;245–71.
- Dutra ER, Oliveira LS, Franca AS, Ferraz VP, Afonso R. A preliminary study on the feasibility of using the composition of coffee roasting exhaust gas for the determination of the degree of roast. J Food Eng. 2001;47(3):241–6.
- Schenker S, Handschin S, Frey B, Perren R, Escher F. Structural properties of coffee beans as influenced by roasting conditions. In: ASIC, 18e colloque, Helsinki. 1999.
- Arya M, Rao LJM. An Impression of Coffee Carbohydrates An Impression of Coffee. 2010;8398(2007).
- Aguiar J, Estevinho BN, Santos L. Trends in Food Science & Technology Microencapsulation of natural antioxidants for food application e The speci fi c case of coffee antioxidants e A review. Trends Food Sci Technol [Internet]. 2016;58:21–39. Available from: http://dx.doi.org/10.1016/j.tifs.2016.10.012
- Stalmach A, Mullen W, Nagai C, Crozier A. On-line HPLC analysis of the antioxidant activity of phenolic compounds in brewed , paper-filtered coffee. 2006;18(figure 1):253–61.
- Binello A, Cravotto G, Menzio J, Tagliapietra S. Polycyclic aromatic hydrocarbons in coffee samples : Enquiry into processes and analytical methods. Food Chem [Internet]. 2021;344(November 2020):128631. Available from: https://doi.org/10.1016/j.foodchem.2020.128631
- Patel AB, Shaikh S, Jain KR, Desai C, Madamwar D. Polycyclic Aromatic Hydrocarbons: Sources, Toxicity, and Remediation Approaches. Vol. 11, Frontiers in Microbiology. Frontiers Media S.A.; 2020.
- Harvey J, Lacey MG. A postsynaptic interaction between dopamine D1 and NMDA receptors promotes presynaptic inhibition in the rat nucleus accumbens via adenosine release. J Neurosci. 1997;17(14):5271–80.
- Purcaro G, Barp L, Moret S. Determination of hydrocarbon contamination in foods. A review. Anal Methods. 2016;8(29):5755–72.
- Singh L, Agarwal T, Simal-Gandara J. PAHs, diet and cancer prevention: Cooking process driven-strategies. Vol. 99, Trends in Food Science and Technology. Elsevier Ltd; 2020. p. 487–506.
- EFSA. Polycyclic Aromatic Hydrocarbons in Food 1 Scientific Opinion of the Panel on Contaminants in the Food Chain Adopted on 9 June 2008. 2008;(June):1–114.
- Lawal AT. Polycyclic aromatic hydrocarbons. A review. Cogent Environ Sci. 2017;3(1):1339841.
- Kacmaz S. Polycyclic aromatic hydrocarbons (PAHs) in flour, bread, and breakfast cereals. In: Flour and Breads and Their Fortification in Health and Disease Prevention. Elsevier; 2019. p. 13–20.
- Pincemaille J, Schummer C, Heinen E, Moris G. Determination of polycyclic aromatic hydrocarbons in smoked and non-smoked black teas and tea infusions. Food Chem. 2014;145:807–13.
- Rose M, Holland J, Dowding A, Petch SRG, White S, Fernandes A, et al. Investigation into the formation of PAHs in foods prepared in the home to determine the effects of frying, grilling, barbecuing, toasting and roasting. Food Chem Toxicol. 2015 Apr 1;78:1–9.
- Houessou JK, Goujot D, Heyd B, Camel V. Modeling the formation of some polycyclic aromatic hydrocarbons during the roasting of Arabica coffee samples. J Agric Food Chem. 2008;56(10):3648–56.
- Huang L, Chen Z, Wen Q, Zhao L, Lee D-J, Yang L, et al. Insights into Feast-Famine polyhydroxyalkanoate (PHA)-producer selection: Microbial community succession, relationships with system function and underlying driving forces. Water Res [Internet]. 2018;131:167–76. Available from: https://www.sciencedirect.com/science/article/pii/S004313541731028X
- Badger GM, Buttery RG. 501. The formation of aromatic hydrocarbons at high temperatures. Part IV. The pyrolysis of styrene. J Chem Soc [Internet]. 1958;2458 – 2463. Available from: https://www.scopus.com/inward/record.uri?eid=2-s2.0-37049056537&doi=10.1039%2FJR9580002458&partnerID=40&md5=ad97898cb22c4394d2f52a4ad7d9e3c0
- Chen BH, Chen YC. Formation of polycyclic aromatic hydrocarbons in the smoke from heated model lipids and food lipids. J Agric Food Chem. 2001;49(11):5238–43.
- Reizer E, Viskolcz B, Fiser B. Formation and growth mechanisms of polycyclic aromatic hydrocarbons: A mini-review. Vol. 291, Chemosphere. Elsevier Ltd; 2022.
- Cross AJ, Freedman ND, Ren J, Ward MH, Hollenbeck AR, Schatzkin A, et al. Meat consumption and risk of esophageal and gastric cancer in a large prospective study. Am J Gastroenterol [Internet]. 2011;106(3):432 – 442. Available from: https://www.scopus.com/inward/record.uri?eid=2-s2.0-79952359390&doi=10.1038%2Fajg.2010.415&partnerID=40&md5=67b5ba31ca6b426d25451a9074cee7fa
- Diggs DL, Huderson AC, Harris KL, Myers JN, Banks LD, Rekhadevi P V, et al. Polycyclic aromatic hydrocarbons and digestive tract cancers: A perspective. J Environ Sci Heal – Part C Environ Carcinog Ecotoxicol Rev [Internet]. 2011;29(4):324 – 357. Available from: https://www.scopus.com/inward/record.uri?eid=2-s2.0-84857857577&doi=10.1080%2F10590501.2011.629974&partnerID=40&md5=78d447307ae58b702d0ba7435499551f
- Iko Afé OH, Saegerman C, Kpoclou YE, Anihouvi VB, Douny C, Igout A, et al. Polycyclic aromatic hydrocarbons contamination of traditionally grilled pork marketed in South Benin and health risk assessment for the Beninese consumer. Food Addit Contam – Part A Chem Anal Control Expo Risk Assess. 2020 May 3;37(5):742–52.
- Khalil A, Villard PH, Dao MA, Burcelin R, Champion S, Fouchier F, et al. Polycyclic aromatic hydrocarbons potentiate high-fat diet effects on intestinal inflammation. Toxicol Lett. 2010 Jul;196(3):161–7.
- Rossnerova A, Rossner P, Milcova A, Topinka J, Ambroz A, Pavlikova J, et al. The impact of polycyclic aromatic hydrocarbons in polluted air and diet on newborns. Toxicol Lett. 2015;2(238):S120.
- Sugimura T, Wakabayashi K, Nakagama H, Nagao M. Heterocyclic amines: Mutagens/carcinogens produced during cooking of meet and fish. Cancer Sci [Internet]. 2004;95(4):290 – 299. Available from: https://www.scopus.com/inward/record.uri?eid=2-s2.0-1942504286&doi=10.1111%2Fj.1349-7006.2004.tb03205.x&partnerID=40&md5=2e4d54bf744264a67ca343446edf9ccf
- Tiwari M, Sahu SK, Pandit GG. Distribution of PAHs in different compartment of creek ecosystem: Ecotoxicological concern and human health risk. Environ Toxicol Pharmacol. 2017 Mar 1;50:58–66.
- Domingo JL, Nadal M. Human dietary exposure to polycyclic aromatic hydrocarbons: A review of the scientific literature. Vol. 86, Food and Chemical Toxicology. Elsevier Ltd; 2015. p. 144–53.
- Lee JG, Suh JH, Yoon HJ. Occurrence and risk characterization of polycyclic aromatic hydrocarbons of edible oils by the Margin of Exposure (MOE) approach. Appl Biol Chem. 2019 Dec 1;62(1).
- Rengarajan T, Rajendran P, Nandakumar N, Lokeshkumar B, Rajendran P, Nishigaki I. Exposure to polycyclic aromatic hydrocarbons with special focus on cancer Asian Pacific Journal of Tropical Biomedicine [Internet]. Vol. 5, Asian Pac J Trop Biomed. 2015. Available from: www.elsevier.com/locate/apjtb
- Bil W, van der Bent SAS, Spiekstra SW, Nazmi K, Rustemeyer T, Gibbs S. Comparison of the skin sensitization potential of 3 red and 2 black tattoo inks using interleukin-18 as a biomarker in a reconstructed human skin model. Contact Dermatitis [Internet]. 2018;79(6):336 – 345. Available from: https://www.scopus.com/inward/record.uri?eid=2-s2.0-85052635020&doi=10.1111%2Fcod.13092&partnerID=40&md5=50af4cfed39b1d07bb20466e9af36042
- Crowell SR, Hanson-Drury S, Williams DE, Corley RA. In vitro metabolism of benzo[a]pyrene and dibenzo[def,p]chrysene in rodent and human hepatic microsomes. Toxicol Lett. 2014 Jul 3;228(1):48–55.
- Perera F, Tang D, Whyatt R, Lederman SA, Jedrychowski W. DNA Damage from Polycyclic Aromatic Hydrocarbons Measured by Benzo[a]pyrene-DNA Adducts in Mothers and Newborns from Northern Manhattan, The World Trade Center Area, Poland, and China [Internet]. 2005. Available from: http://aacrjournals.org/cebp/article-pdf/14/3/709/2263240/709-714.pdf
- Tarantini A, Maître A, Lefèbvre E, Marques M, Rajhi A, Douki T. Polycyclic aromatic hydrocarbons in binary mixtures modulate the efficiency of benzo[a]pyrene to form DNA adducts in human cells. Toxicology. 2011 Jan 11;279(1–3):36–44.
- Lewtas J. Air pollution combustion emissions: Characterization of causative agents and mechanisms associated with cancer, reproductive, and cardiovascular effects. Vol. 636, Mutation Research – Reviews in Mutation Research. 2007. p. 95–133.
- Onopiuk A, Kołodziejczak K, Szpicer A, Wojtasik-Kalinowska I, Wierzbicka A, Półtorak A. Analysis of factors that influence the PAH profile and amount in meat products subjected to thermal processing. Vol. 115, Trends in Food Science and Technology. Elsevier Ltd; 2021. p. 366–79.
- Schwerdtle T, Ebert F, Thuy C, Richter C, Mullenders LHF, Hartwig A. Genotoxicity of soluble and particulate cadmium compounds: Impact on oxidative dna damage and nucleotide excision repair. Chem Res Toxicol. 2010 Feb 15;23(2):432–42.
- Corsini E, Van Loveren H. Molecular Immunotoxicology. Wiley; 2014.
- Amirdivani S, Khorshidian N, Dana G, Mohammadi R, Amir M, Lorena S, et al. Polycyclic aromatic hydrocarbons in milk and dairy products. 2019;72(1).
- Celik-Saglam I, Balcik C, Cetin B. Concentrations, sources, and risk assessment of polycyclic aromatic hydrocarbons (PAHs) in black, green and fruit flavored tea in Turkey. J Food Compos Anal. 2022 Jun 1;109.
- Gerde P, Muggenburg BA, Lundborg M, Dahl AR. The rapid alveolar absorption of diesel soot-adsorbed benzo[a]pyrene: bioavailability, metabolism and dosimetry of an inhaled particle-borne carcinogen and 2 Battelle association warrants further investigation. Vol. 22, Carcinogenesis. 2001.
- Bendtsen KM, Bengtsen E, Saber AT, Vogel U. A review of health effects associated with exposure to jet engine emissions in and around airports. Vol. 20, Environmental Health: A Global Access Science Source. BioMed Central Ltd; 2021.
- Kropachev K, Kolbanovskiy M, Liu Z, Cai Y, Zhang L, Schwaid AG, et al. Adenine-DNA adducts derived from the highly tumorigenic dibenzo[a,l]pyrene are resistant to nucleotide excision repair while guanine adducts are not. Chem Res Toxicol. 2013 May 20;26(5):783–93.
- Zhou GD, Richardson M, Fazili IS, Wang J, Donnelly KC, Wang F, et al. Role of retinoic acid in the modulation of benzo(a)pyrene-DNA adducts in human hepatoma cells: Implications for cancer prevention. Toxicol Appl Pharmacol. 2010 Dec 15;249(3):224–30.
- Olivier M, Hollstein M, Hainaut P. TP53 mutations in human cancers: origins, consequences, and clinical use. Cold Spring Harb Perspect Biol [Internet]. 2010;2(1):a001008. Available from: https://www.scopus.com/inward/record.uri?eid=2-s2.0-77955363995&doi=10.1101%2Fcshperspect.a001008&partnerID=40&md5=813f5a7511da5c6fcf3a04ef00ccb9cb
- Delft JHM Van, Mathijs K, Staal YCM, Herwijnen MHM Van, Brauers KJJ, Kleinjans JCS. Time Series Analysis of Benzo [ A ] Pyrene-Induced Transcriptome Changes Suggests That a Network of Transcription Factors Regulates the Effects on Functional Gene Sets. 2010;117(2):381–92.
- Miller KP, Ramos KS. Impact of cellular metabolism on the biological effects of benzo [a] pyrene and related hydrocarbons. Drug Metab Rev. 2001;33(1):1–35.
- Pareja L, Fernández-Alba AR, Cesio V, Heinzen H. Analytical methods for pesticide residues in rice. Vol. 30, TrAC – Trends in Analytical Chemistry. 2011. p. 270–91.
- Bozkurt SS, Merdivan M, Erdem P, Altınıs A. Talanta Chitosan and dicationic ionic liquid intercalated clay-coated solid-phase microextraction fiber for determination of sixteen polycyclic aromatic hydrocarbons in coffee and tea samples. 2021;235(July).
- Singh L, Agarwal T. Comparative analysis of conventional and greener extraction methods and method validation for analyzing PAHs in cooked chicken and roasted coffee. Food Chem [Internet]. 2021;364(June):130440. Available from: https://doi.org/10.1016/j.foodchem.2021.130440
- Bishnoi NR, Mehta U, Sain U, Pandit GG. Quantification of polycyclic aromatic hydrocarbons in tea and coffee samples of Mumbai City (India) by high performance liquid chromatography. Environ Monit Assess. 2005;107(1–3):399–406.
- Houessou JK, Benac C, Delteil C, Camel V. Determination of polycyclic aromatic hydrocarbons in coffee brew using solid-phase extraction. J Agric Food Chem. 2005;53(4):871–9.
- Kamal El-Deen A, Shimizu K. Modified μ-QuEChERS coupled to diethyl carbonate-based liquid microextraction for PAHs determination in coffee, tea, and water prior to GC–MS analysis: An insight to reducing the impact of caffeine on the GC–MS measurement. J Chromatogr B Anal Technol Biomed Life Sci [Internet]. 2021;1171(January):122555. Available from: https://doi.org/10.1016/j.jchromb.2021.122555
- Wu H, Li D, Zhao B, Guan S, Jing X, Ding Y, et al. Magnetic covalent organic framework nanocomposites as a new adsorbent for the determination of polycyclic aromatic hydrocarbons in water and food samples. Anal Methods. 2021;13(25):2847–56.