FERMENTAÇÃO DE PIMENTA HABERANO LARANJA (CAPSICUM CHINENSE L): CARACTERIZAÇÃO FÍSICO-QUÍMICA E CAPACIDADE ANTIOXIDANTE
Capítulo de livro publicado no livro PROCESSAMENTO DE ALIMENTOS: PESQUISAS E INOVAÇÕES PARA NOVOS PRODUTOS. Para acessa-lo clique aqui.
DOI: https://doi.org/10.53934/202311-02
Este trabalho foi escrito por:
Virgínia Mirtes de Alcântara Silva , Newton Carlos Santos ,
Mailson Gregório Gonçalves , Michael Marcos de Aquino Gomes , Vitória Régia do Nascimento Lima ,Sara Morgana Félix de Sousa ,
Dauany de Sousa Oliveira
Introdução
A busca por alimentos funcionais e ingredientes naturais com propriedades benéficas à saúde tem ganhado crescente atenção nos últimos anos (Swallah et al., 2023). Nesse contexto, as pimentas habanero (Capsicum chinense L) têm se destacado devido às suas características únicas e potencial valor nutricional. Além de conferirem sabor e pungência aos alimentos, essas pimentas também têm sido associadas a uma série de benefícios à saúde, graças à presença de compostos bioativos, como os antioxidantes (Aryee et al., 2022).
A pimenta Habanero é uma planta herbácea ou arbustiva, ramificada, atingindo um porte de até 2,5 metros de altura. Os espécimes imaturos de pimentas habanero são verdes, mas sua cor varia na maturidade. As cores mais comuns são o laranja (semi-maduro) e o vermelho quando maduro. Segundo pesquisas científicas, as origens da pimenta habanero encontram-se na zona que se estende do sul do Brasil ao norte da Argentina, passando pelo leste da Bolívia e oeste do Paraguai (González-Toxqui et al., 2020).
A fermentação é um processo tradicionalmente utilizado para preservar alimentos e melhorar suas características sensoriais e nutricionais. Alimentos fermentados são alimentos nutricionalmente e funcionalmente ricos produzidos pela ação microbiana associada a bactérias, leveduras, fungos miceliais e suas enzimas (Nithya et al., 2023). No caso das pimentas habanero laranja, a fermentação pode não apenas prolongar sua vida útil, mas também alterar sua composição química, levando a mudanças na concentração de compostos antioxidantes e outros metabólitos (Aryee et al., 2022).
Neste contexto, o presente estudo tem como objetivo avaliar o efeito da concentração de sal nas características físico-química e antioxidantes das pimentas habanero laranja submetidas ao processo de fermentação, incluindo a determinação de parâmetros como pH, acidez titulável. Além disso, busca-se avaliar a capacidade antioxidante dessas pimentas fermentadas, por meio de ensaios como ABTS e DPPH. A compreensão dos efeitos da fermentação na composição e propriedades das pimentas habanero laranja pode contribuir para sua utilização mais ampla na indústria de alimentos e nutracêuticos, oferecendo produtos com valor agregado e benefícios à saúde.
Materiais e Métodos
Preparo das amostras Inicialmente, as pimentas habareno laranja foram selecionadas e higienizadas para eliminar impurezas e com auxílio de uma faca seus talos foram removidos. Após higienização, as pimentas foram cortas em finas fatias com dimensões não definidas (Figura 1).

Foram utilizadas porções de aproximadamente 100g de pimenta, as quais foram acondicionadas em frascos de vidro. Em cada frasco, foram adicionados 4, 6 e 8% de sal, juntamente com 1,5 L de água, e agitados para homogeneização (Figura 2).
Os frascos foram hermeticamente fechados com suas respectivas tampas e selados com fita, sendo então submetidos a um processo de fermentação natural, sem a adição de qualquer cultura iniciadora. Esse período de fermentação ocorreu ao longo de 4 semanas, em condições de temperatura ambiente.
Caracterização das formulações
Determinação de pH e acidez titulável
O valor do pH foi medido diretamente usando um medidor de pH à 20 °C após uma calibração usando as soluções tampão padrão com valores de pH de 4,01, 6,86 e 9,18, respectivamente. Para estimar a acidez titulável, o método de titulação de NaOH 0,1 N. Para isso, 10 g de amostras de pimenta em fermentação e trazendo o pH para 8,2. Uma gota do indicador fenolftaleína foi adicionada à solução e titulada com NaOH 0,1 N até atingir a coloração rosa (AOAC, 2016).
Determinação de compostos fenólicos totais
Método de Folin-Ciocalteu descrito por Chang et al. (2006) foi usado para determinar o teor de compostos fenólicos totais. Para isso, um extrato aquoso foi preparado na proporção 1:10 (fermentado:água). Uma alíquota de 125 μL do extrato foi misturada com 500 μL de água destilada e misturada com 125 μL do reagente Folin ciocalteu por 6 min. Em seguida, foram adicionados 1,25 mL de Na2CO 3 7% e 1 mL de água destilada e finalmente incubados à temperatura ambiente no escuro por 30 min. A absorbância foi medida a 760 nm usando um espectrofotômetro UV/VIS e os resultados foram expressos em mg de equivalente ácido gálico (EAG)/100g de amostra usando uma curva padrão.
Determinação da atividade antioxidante
Dois diferentes métodos (ABTS e DPPH) foram usados para determinar a atividade antioxidante de acordo com o protocolo descrito por Thaipong et al. (2006). O mesmo extrato descrito na análise de compostos fenólicos totais usado. Para todos os métodos de determinação de antioxidantes, os resultados foram expressos em µMol Trolox/g de amostra a usando uma curva padrão de Trolox (0–200 mg/l).
Análise estatística
A análise de variância (ANOVA) no nível de 0,05 (p < 0,05) foi realizada para determinar a significância estatística entre as amostras por meio do software Statistic 8.0.
Resultados e Discussões
A Figura 1 ilustra a variação dos valores de pH ao longo do período de fermentação das pimentas em diferentes concentrações de sal. A análise da variação do pH ao longo do tempo fornece insights importantes sobre a dinâmica da fermentação e seu impacto nas características físico-químicas das pimentas.
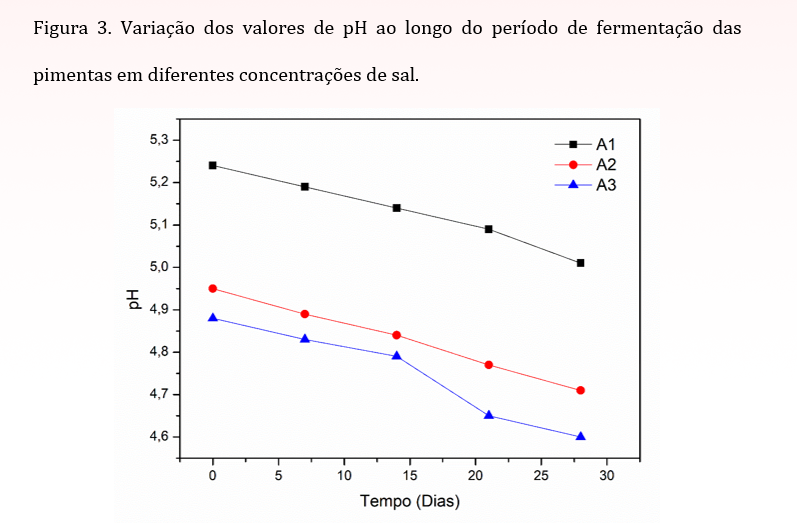
Durante a avaliação do pH das amostras ao longo de 28 dias de fermentação das pimentas em diferentes concentrações de sal, observou-se um decréscimo nos valores de pH. Na formulação contendo 4% de sal, os valores de pH diminuíram de 5,24 para 5,01. Para a formulação com 6% de sal, ocorreu uma redução dos valores de pH de 4,95 para 4,71. Já na formulação com 8% de sal, os valores de pH decresceram de 4,88 para 4,60 ao longo do período de 28 dias de armazenamento.
Essas reduções observadas nos valores de pH ao longo do período de fermentação podem ser atribuídas ao processo de acidificação que ocorre durante a fermentação das pimentas. O ácido lático, produzido como subproduto do metabolismo microbiano, é um dos principais responsáveis por essa acidificação. Conforme as bactérias lácticas e outros microorganismos presentes na fermentação metabolizam os açúcares presentes nas pimentas, o ácido lático é produzido, levando a uma diminuição gradual do pH (Delgado-Ospina et al., 2020). A concentração de sal nas formulações também pode influenciar essa acidificação, visto que as bactérias lácticas são mais eficientes na produção de ácido lático em ambientes com teores moderados de sal (Liu et al., 2023).
A Figura 4 apresenta a variação dos valores de acidez titulável ao longo do período de fermentação das pimentas em diferentes concentrações de sal. Durante o período de 28 dias de fermentação, foi notado um aumento significativo nos valores de acidez das amostras. Na formulação com 4% de sal, os valores de acidez aumentaram de 0,52% para 0,81%. Na formulação com 6% de sal, esse valor aumentou de 0,64% para 0,90%, e na formulação com 8% de sal, a acidez subiu de 0,66% para 1,03%.
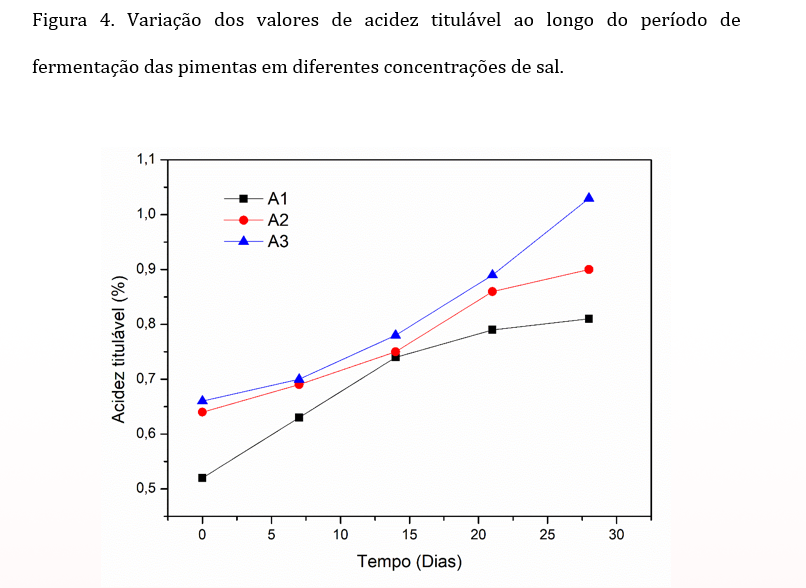
Esses resultados demonstram um comportamento inverso em relação aos valores de pH, porém, estão em acordo com o processo de fermentação. Esse aumento na acidez é um indicativo da conversão dos açúcares presentes nas pimentas em ácidos, contribuindo para o desenvolvimento do perfil sensorial característico das pimentas fermentadas (Bely et al., 2023).
A Tabela 1 apresenta os resultados da análise dos compostos fenólicos totais e da atividade antioxidante nas amostras de pimentas fermentadas em diferentes concentrações de sal. Esses parâmetros são indicativos importantes da presença de componentes bioativos com potencial benefício à saúde.
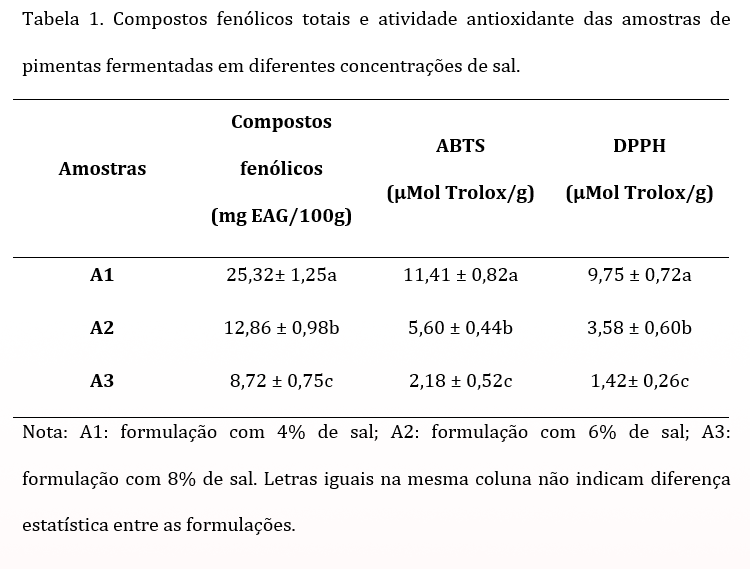
Os teores de compostos fenólicos variaram de 8,72 a 25,32 mg EAG/100g e demonstraram significativa diferença estatística entre as diferentes concentrações de sal (p<0,05). Notavelmente, uma redução nos valores foi observada à medida que a concentração de sal aumentou de 4% para 8%. Uma explicação plausível para essa diminuição reside na influência do sal sobre a atividade enzimática e metabólica das pimentas durante o processo de fermentação. Além disso, o aumento na concentração de sal pode impactar a estrutura celular das pimentas, ocasionando alterações nas vias metabólicas e na composição química celular. Essas alterações podem afetar a disponibilidade de precursores e substratos essenciais para a síntese de compostos fenólicos.
Os resultados da atividade antioxidante revelaram variações significativas, com valores oscilando de 2,18 a 11,41 µmol Trolox/g para o ensaio ABTS e de 1,42 a 9,75 µmol Trolox/g para o ensaio DPPH. É notável que os valores mais elevados de atividade antioxidante foram observados nas formulações com concentrações mais baixas de sal (A1) indicando uma possível relação inversa entre a concentração de sal e a atividade antioxidante. Esse padrão pode ser atribuído à capacidade antioxidante intrínseca dos compostos fenólicos presentes nas pimentas, os quais desempenham um papel crucial na neutralização de radicais livres e outros agentes oxidantes.
Considerações finais
Em suma, este estudo investigou o efeito da concentração de sal na fermentação de pimentas, analisando suas alterações físico-químicas e atividade antioxidante. Os resultados indicaram um processo de acidificação das amostras ao longo do período de fermentação, acompanhado por um aumento na acidez titulável. Esse comportamento inverso em relação aos valores de pH evidencia a conversão dos açúcares em ácidos durante a fermentação. Além disso, a análise dos compostos fenólicos totais e da atividade antioxidante revelou uma relação entre a concentração de sal e esses parâmetros, com uma diminuição nos valores à medida que a concentração de sal aumentou. Notavelmente, as formulações com concentrações mais baixas de sal exibiram maior atividade antioxidante, indicando o potencial dessas pimentas fermentadas como fonte de antioxidantes naturais.
Referências
A.O.A.C. (2016). Official methods of analysis of AOAC International (20th ed.). Rockville, Maryland, USA: AOAC international.
Aryee, A. N., Owusu-Kwarteng, J., Senwo, Z., & Alvarez, M. N. (2022). Characterizing fermented habanero pepper (Capsicum chinense L). Food Chemistry Advances, 1, 100137.
Bely, M., Rinaldi, A., & Dubourdieu, D. (2003). Influence of assimilable nitrogen on volatile acidity production by Saccharomyces cerevisiae during high sugar fermentation. Journal of bioscience and bioengineering, 96(6), 507-512.
Chang, C. H., Lin, H. Y., Chang, C. Y., & Liu, Y. C. (2006). Comparisons on the antioxidant properties of fresh, freeze-dried and hot-air-dried tomatoes. Journal of food engineering, 77(3), 478-485.
Delgado-Ospina, J., Di Mattia, C. D., Paparella, A., Mastrocola, D., Martuscelli, M., & Chaves-Lopez, C. (2020). Effect of fermentation, drying and roasting on biogenic amines and other biocompounds in Colombian Criollo cocoa beans and shells. Foods, 9(4), 520.
González-Toxqui, C., González-Ángeles, Á., López-Avitia, R., & González-Balvaneda, D. (2020). Drying habanero pepper (Capsicum chinense) by modified freeze drying process. Foods, 9(4), 437.
Liu, H., Yang, S., Liu, J., Lu, J., & Wu, D. (2023). Effect of salt concentration on Chinese soy sauce fermentation and characteristics. Food Bioscience, 102825.
Nithya, A., Misra, S., Panigrahi, C., Dalbhagat, C. G., & Mishra, H. N. (2023). Probiotic potential of fermented foods and their role in non-communicable diseases management: An understanding through recent clinical evidences. Food Chemistry Advances, 3, 100381.
Thaipong, K., Boonprakob, U., Crosby, K., Cisneros-Zevallos, L., & Byrne, D. H. (2006). Comparison of ABTS, DPPH, FRAP, and ORAC assays for estimating antioxidant activity from guava fruit extracts. Journal of food composition and analysis, 19(6-7), 669-675.