ESTUDO DO CONGELAMENTO DE POLPA DE SERIGUELA E SPIRULINA
Capítulo de livro publicado no livro PROCESSAMENTO DE ALIMENTOS: PESQUISAS E INOVAÇÕES PARA NOVOS PRODUTOS. Para acessa-lo clique aqui.
DOI: https://doi.org/10.53934/202311-09
Este trabalho foi escrito por: Álison Bruno Borges de Sousa*
Autor correspondente: [email protected]
Introdução:
Na Zona da Mata Paraibana são encontradas naturalmente as frutíferas exóticas subutilizadas e ainda em domesticação, entre elas o gênero Spondias e Hancornia todas com enorme potencial para exploração comercial (GONDIM et al., 2013). Em relação às propriedades nutricionais, as Spondias são ricas em vitaminas (B1, B2, B3, A e C), minerais (cálcio, potássio, ferro e fósforo) e ainda possuem alta concentração de carotenoides e taninos, os quais estão relacionados à sua capacidade antioxidante (VIDIGAL et al., 2011).
Dentre a espécie que se destacam ao gênero está a seriguela (Spondias purpurea L.), planta nativa da América Central, popularmente conhecida como: ciriguela, ameixa espanhola, cajá vermelho, jacote, ciruela mexicana (SILVA, 2011). Essa fruta desponta no nordeste brasileiro como uma excelente opção econômica para inúmeros produtores. Devido sua qualidade as frutas são consumidas in natura, ou utilizadas no preparo de polpa concentrada, de bebidas fermentadas, vinho, sucos e sorvetes (FREIRE, 2001).
O uso de combinação de ingredientes com apelo de melhoria da qualidade nutricional dos alimentos é atualmente explorado devido às novas exigências dos consumidores por produtos com alto valor nutritivo e benéficos à saúde. Um dos mecanismos possíveis de se agregar valor aos frutos e seus derivados é incrementando-os através da combinação com outros ingredientes, como por exemplo as microalgas, as quais possuem alto valor proteico e de atividade antioxidante.
Dentre as microalgas, a mais comumente estudada é a Spirulina platensis cuja biomassa obtida sendo investigada como fonte proteica de elevado valor biológico. Tem sido consumida como suplemento alimentar, porém o uso como componente para desenvolvimento de alimentos funcionais se mostra promissor. Assim, os estudos têm sido direcionados para a avaliação de moléculas bioativas com potenciais ações promotoras da saúde humana e animal (MORAIS et al., 2015; HADDAR et al., 2012).
Tanto a polpa de seriguela quanto a Spirulina são alimentos perecíveis e que necessitam de técnicas de conservação para garantir a manutenção da qualidade do produto durante seu período de armazenamento.
O conhecimento das propriedades térmicas de polpa congelada é essencial para calcular a distribuição de temperatura durante o congelamento e armazenamento congelado. Os engenheiros de alimentos estão interessados em prever tempos de congelamento, a fim de estimar a refrigeração, requisitos para os sistemas de congelamento e para projetar equipamento necessário para um processamento eficaz. Energia, eficiência, confiabilidade, segurança e qualidade do produto final também devem ser considerados (DELGADO e SUN, 2001).
O tempo do processo é o fator de maior criticidade para a escolha de um sistema de congelamento, devido às diferenças da temperatura inicial, no tamanho e forma dos alimentos, no ponto de congelamento e na taxa de formação dos cristais de gelo entre diferentes pontos de um mesmo alimento. Além de mudanças na densidade, condutividade térmica, calor específico e na difusividade térmica com a redução de temperatura do alimento (FELLOWS, 2006). Para a eficiência do sistema de congelamento é imprescindível o conhecimento do tempo despendido para este processo. Os requisitos para o tempo de congelamento estabelecem a capacidade do sistema e influenciam diretamente na qualidade do produto (CAVALCANTI MATA et al., 2003).
Portanto o objetivo nesta pesquisa foi estudar a cinética de congelamento de formulações contendo diferentes concentrações de maltodextrina em polpa mista de seriguela e Spirulina, em três temperaturas (-25, -50 e -75 ºC), determinando sua difusividade térmica efetiva e energia de ativação.
Material e Métodos:
Utilizou-se para a realização desta pesquisa, Seriguela em estádio de maturação maduro, adquirida em um único fornecedor no município de Campina Grande. Também empregou-se Spriulina platensis em pó, obtida na Fazenda Tamanduá, Santa Terezinha-PB e maltodextrina MOR-REX®1910, dextrose equivalente 10 da Ingredion.
Após as etapas de seleção, lavagem e higienização em água clorada a 50 ppm de cloro ativo por 15 minutos, os frutos foram despolpados em despolpadeira horizontal com malha de 2 mm de abertura com o intuito de obter um produto uniforme. A polpa foi homogeneizada e embalada em sacos de polietileno de baixa densidade com volume de 200 mL, em seguida congelada e armazenada em câmara frigorífica a -18 ºC até o momento da realização do experimento.
As amostras foram distribuídas em sacos de polietileno, contendo aproximadamente 100 gramas de amostra, seladas e medidas o comprimento, largura e altura em milímetros da amostra a ser congelada.
Visando determinar a curva de congelamento introduziu-se no centro geométrico da placa plana um termopar de 0,2 mm de diâmetro acoplado a um registrador Digi-Sensi de dois canais; o outro termopar foi introduzido no interior da unidade de congelamento cuja finalidade foi monitorar o meio congelante, de modo a se determinar o instante de equilíbrio térmico para cada temperatura de congelamento.
Para o estudo da cinética de congelamento das formulações na temperatura de -25 ± 2 ºC, foi utilizado um freezer horizontal e os dados coletados a cada 60 segundos, para as temperaturas de -50 e -75 ± 2 ºC utilizou-se um balcão criogênico horizontal e os dados foram obtidos a cada 10 s. Todos os dados foram coletados em triplicata.
Aplicou-se aos dados experimentais a Lei de Fourier, onde o número de Fourier (F0) é o tempo adimensional, em função do comprimento característico L para superfície plana, ou do raio externo para cilindros ou esferas, conforme Equação 3.1:
Para calcular a transferência de calor, em regime transiente, cuja forma se assemelha a uma placa plana de espessura 2L, pequena em função do tamanho da mesma, ou seja, placa infinita, inicialmente à temperatura Ti é subitamente colocada em um meio fluido com temperatura Tinf, ocorrerá transferência de energia por condução e convecção entre o corpo e o meio, sendo a distribuição de temperatura Tx numa posição “x” qualquer, desse corpo, uma função do tempo, fornecida pela Equação abaixo que equivale ao modelo de Fourier:
Para o ajuste do modelo foram realizadas análises de regressão não linear, pelo método Gauss-Newton. Para cada modelo foi considerado o coeficiente de determinação (R2), utilizando o Software STATISTICA 7.0®.
Resultados e Discussão
Observam-se na Figura 3.2 as curvas de congelamento para polpa de seriguela com Spirulina sem adição de maltodextrina nas temperaturas de -25, -50 e -75 °C. Verificou-se a presença das três fases do congelamento, sendo a fase I (resfriamento), fase II (cristalização ou congelamento) e a fase III (pós-congelamento). Comportamento similar ao que ocorre no congelamento da água pura, podendo-se justificar pelo alto teor de água do material (80,34%).
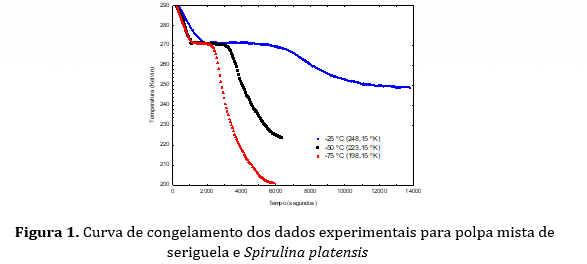
A fase I compreende a etapa de resfriamento do produto até o início do congelamento. Para a temperatura de -25 ºC o controle obteve-se tempo de 1.600 segundos, enquanto que nas temperaturas de -50 ºC e -75 ºC os tempos da fase I foram menores.
A temperatura de início de congelamento (Tic) foi determinada quando se deu início a Fase II (nucleação). Os valores de Tic encontrados para o Controle foram de -1,7; -1,8 e -1,9 ºC, respectivamente para -25, -50 e -75 ºC. Os valores experimentais determinados estão coerentes com os especificados na literatura: polpa de morango congelada a -20 ºC apresentou Tic =-0,7 ºC (FERNANDES et al., 2010); congelamento de mangaba obteve Tic = -1,0 ºC (SOARES et al., 2012); e o congelamento de polpa de acerola a -25 ºC exibiu Tic = -1,1ºC (PEREIRA, 2013).
A temperatura de início do congelamento de soluções ideais de mono e bicomponentes pode ser descrita pela lei de Raoult e a especificidade de polpas de frutas, principalmente com adição de sólidos, necessita de investigações específica para o estudo da temperatura do início de congelamento para cada produto. Tic para sistemas de polpas de frutas depende dos mesmos fatores descritos para as soluções ideais, sendo o teor de sólidos de importância básica. Quanto mais alto for o teor de sólido mais baixo será o ponto de congelamento incipiente (FERREIRA; GUIMARÃES e MAIA, 2007).
Durante a Fase II, acontece o congelamento propriamente dito da água no material biológico, sua nucleação. Nesta fase ocorre o aumento dos cristais de gelo e remoção do calor latente, assim como o aumento da concentração dos sólidos solúveis (SOARES et al., 2012). O tempo total de cristalização reduziu proporcionalmente à redução de temperatura de congelamento, constatando-se valores de 3.420 s (-25 ºC), 1.920 s (-50 ºC) e 1.200 s (-75 ºC).
A Fase III corresponde ao pós-congelamento, no qual acontece a diminuição de temperatura do produto já congelado (CAVALCANTI MATA et al., 2005). O tempo total registrado foi de 11.820, 4.500 e 4.440 segundos para -25, -50 e -75 ºC, respectivamente. O tempo de cristalização reduziu com o aumentou do gradiente de temperatura, como esperado. As temperaturas de -50 e -75 ºC apresentaram comportamento semelhante para esta fase.
Estudos científicos sobre o comportamento do congelamento de frutos corroboram com a verificação as três fases bem definidas. Como observado por Araújo, Braga e Cavalcanti Mata (2000) em cinética de congelamento de polpa de acerola a baixas temperaturas; por Cavalcanti Mata, Braga e Silva (2003) no congelamento de frutos de cajá a temperaturas semi-criogênicas; por Cavalcanti Mata et al. (2005) no congelamento de polpa de graviola a -50 °C.
Na Tabela 3.2 encontram-se os parâmetros de espessura (L), fator de atraso (J) coeficiente de difusão, coeficiente do modelo (K), difusividade efetiva (⍺), difusividade efetiva média, coeficiente de determinação (R2), erro médio estimado (SE) e erro médio relativo (P%) desvio-padrão da estimativa para polpa de seriguela com Spirulina nos estágios de congelamento a -25, -50 e -75 ºC.
Verificou-se que os valores de difusividade efetiva média nas formulações aumentaram com a redução da temperatura de congelamento. O valor da difusividade média obtido na temperatura de -25 ºC foi de 1,19 mm2.s-1, enquanto que para a temperatura de -75 ºC foi de 2,81 mm2.s-1. Tem-se que a difusividade térmica efetiva média é mais elevada quando o produto é submetido a um gradiente térmico maior, ou seja, a difusividade térmica aumenta com a diminuição de temperatura de congelamento. Araújo, Braga e Cavalcanti Mata (2000) obtiveram valores de difusividade média de 1,23, 10,77 e 39,32 mm2.s-1 para polpa de acerola congelada à -22,6ºC, -100ºC e -196°C respectivamente.
O fator de atraso (J) nas Fases I e III apresentaram valores acima do ciclo logarítmico, enquanto que na Fase II, os valores de J mantiveram-se abaixo do ciclo logarítmico refletindo em influência não significativa na αm.
Na figura 2 encontra-se a relação da difusividade térmica efetiva em função da temperatura em K. A equação utilizada foi a de Arrhenius, empregada para explicar as reações químicas. A ocorrência de uma reação química está relacionada, obrigatoriamente, com o contato entre as moléculas reagentes e a uma energia mínima necessária. Esta energia mínima para a ocorrência da reação é chamada energia de ativação (Ea); portanto, pode-se utilizar a equação de Arrhenius para determinar a energia de ativação do processo de congelamento, entendendo que esta seria a energia mínima necessária para que ocorram os rearranjos moleculares com vista à formação das estruturas congeladas (CAVALCANTI-MATA et al., 2012). Podendo assim ser aplicada ao congelamento da polpa mista de seriguela com Spirulina platensis.
Tabela no livro
Conclusões
Foi possível verificar as três fases do processo de congelamento bem definidas nas amostras, fase I (pré-congelamento), fase II (cristalização) e fase III (pós-congelamento) em todas as temperaturas estudadas. Ressalta-se que quanto mais alta a temperatura, mais distintas encontravam-se as fases de congelamento. O tempo de congelamento foi inversamente proporcional ao gradiente térmico, ou seja, quanto maior o gradiente térmico, menor o tempo de congelamento das amostras de polpa mista de seriguela com Spirulina platensis, para as temperaturas de -25, -50 e -75 ºC. A difusividade média efetiva da polpa mista de seriguela com Spirulina platensis aumentou com a diminuição da temperatura de congelamento, sendo os coeficientes de determinação superiores a 96,80%. A foi crescente à medida que se adicionou maltodextrina na polpa mista de seriguela com Spirulina platenis. A equação de Arrhenius se ajustou bem aos dados da energia de ativação, com coeficientes de determinação superiores a 88,41%.
Referências
ARAÚJO, M. S. O.; BRAGA, M. E. D.; CAVALCANTI MATA, M. E. R. M. Cinética de congelamento de polpa de acerola a baixas temperaturas. Revista Brasileira de Produtos Agroindustriais, v.2, n.1, p.27-34, 2000.
BODNER, G. M.; NAKHLEH, M. B.; ROBINSON, W. R. Activation energy. The chemical education web site. Division of Chemical Education at Purdue University, West Lafayette, IN, USA. In: http://w3.ufsm.br/juca/activate.htm. 19 Abr. 2018.
CAVALCANTI MATA, M. E. R. M. MORAIS, J. O.; DUARTE, M. E. M.; FARIAS, P. A.; QUEIROZ, A. J. M. Cinética de congelamento do feijão (Phaseolus vulgaris L.) a baixas temperaturas. Revista Brasileira de Engenharia Agrícola e Ambiental, v.16, n.6, p.667–674, 2012.
CAVALCANTI MATA, M. E. R. M.; BRAGA, M. E. D.; SILVA, M. Curvas de congelamento de frutos de cajá (Spondias lutea L.). Revista Brasileira de Produtos Agroindustriais, Campina Grande Especial, n.1, p.55-62, 2003.
CAVALCANTI MATA, M. E. R. M.; DUARTE, M. E. M., ALSEMO, G. C. S., RODRIGUES, E., GUEDES, M. A., CAVALCANTI, A. S. R. R. M.; OLIVEIRA, C. C. A. Obtenção de Graviola em pó pelo processo de Liofilização. Revista Brasileira de Produtos Agroindustriais, v. 7, n.2, p.165-172, 2005.
DELGADO, A.E.; SUN, D.W. Heat and mass transfer models for predicting freezing process – a review. Journal of Food Engineering, Davis, v. 47, p. 157-174, 2001.
FELLOWS, P. J. Tecnologia do processamento de alimentos: princípios e prática.2 ed. Porto Alegre: Artmed, 2006. 430 p.
FERNANDES, T. N.; RESENDE, J. V.; CRUVINEL, R. S. R.; RENO, M. J. Relação entre o comportamento reológico e a dinâmica do congelamento e descongelamento de polpa de morango adicionada de sacarose e pectina. Ciência e Tecnologia de Alimentos, Campinas, v. 30, n. 1, p. 188-204, jan-mar, 2010.
FERREIRA, G. M.; GUIMARÃES, M. J. O. C.; MAIA, M. C. A. Interações sinérgicas entre polpa de fruta e polissacarídeos em cisalhamento estacionário e dinâmico. In: ENCONTRO REGIONAL SUL DECIÊNCIA E TECNOLOGIA DE ALIMENTOS, 9, 2007, Curitiba.Anais… Curitiba: Editora TecArt, 2007. p. 654-660.
FREIRE, F. C. O. Uso da manipueira no controle do oídio da cerigueleira: resultados e preliminares. Comunicado Técnico, v. 70, p.1-3, 2001.
GONDIM, P. J. S.; SILVA, S. M.; PEREIRA, W. E.; DANTAS, A. L.; CHAVES NETO, J. R.; SANTOS, L. F. Qualidade de frutas de acessos de umbu-cajazeira (Spondias sp.). Revista Brasileira de Engenharia Agrícola e Ambiental, v. 17, p. 1217-1221, 2013.
MORAIS, M. G.; VAZ, B. S.; MORAIS, E. G.; COSTA, J. A. V. Biologically active metabolites synthesized by microalgae (Report). BioMed Research International, v. 2015, p. 1–15, 2015.
PEREIRA, C. G. Propriedades termofísicas e comportamento reológico de polpa de acerola em diferentes concentrações e temperaturas. 2013. 135 p. Dissertação (Mestrado em Ciência de Alimentos), Universidade Federal de Lavras, Minas Gerais.
SILVA, B. M., SANTOS, R. P., MENDES, L. S., PINHO, P. G., VALENTÃO, P., ANDRADE, P. B., et al. Dracaena draco L. fruit: phytochemical and antioxidant activity assessment. Food Research International, v. 44, p. 2182–2189, 2011.
SOARES, D. S. C.; SANTOS, J. T. S.; CAMPOS, A. F. P.; COSTA, F. S. C.; NUNES, T. P.; OLIVEIRA JÚNIOR, A. M. Avaliação do congelamento de mangada (Hancornia Speciosa Gomes) em ultrafreezer através dos modelos matemáticos de Planck e Pham. Scientia Plena, v. 8, n. 4, 2012.
VIDIGAL, M. C.T. R.; MINIM, V. P. R.; CARVALHO, N. B.; MILAGRES, M. P.; GONÇALVES, A. C. A. Effect a health claim on consumer acceptance of exotic Brazilian fruit juices: acai (Euterpe oleracea), camu-camu (Myrciaria dubia), cajá (Spondias lutea L.) and umbu (Spondias tuberosa A.). Food Research International, v. 44, nº 7, p.1988 – 1996, 2011.